Diagrama de Fases
O diagrama de fases é um gráfico que permite definir em que estado físico uma substância se encontra num dado instante, conhecendo sua temperatura e pressão.
Medidas feitas em laboratório são utilizadas para construir o diagrama de fases de uma determinada substância.
O diagrama é dividido em três regiões, que representam o estado sólido, líquido e vapor.
Os pontos das linhas que delimitam essas regiões indicam os valores de temperatura e pressão que a substância pode estar em dois estados.
Um diagrama de fases apresenta os seguintes elementos:
- Curva de fusão: separa as áreas que correspondem aos estados sólido e líquido.
- Curva de vaporização: separa as áreas que correspondem as fases líquida e vapor.
- Curva de sublimação: separa as áreas que correspondem as fases sólida e vapor.
- Ponto triplo: ponto de interseção das três curvas (fusão, vaporização e sublimação). Este ponto indica os valores de temperatura e pressão que a substância pode simultaneamente estar nos três estados.
- Ponto crítico: indica a maior temperatura que a substância é vapor. A partir desse ponto não é mais possível diferenciar os estados líquido e vapor. Para temperaturas acima do ponto crítico a substância passa a ser um gás.
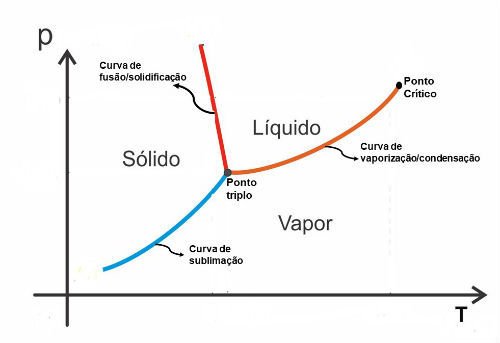
Na figura abaixo, apresentamos uma representação de um diagrama de fases:
Leia mais em: Mudanças de estado físico.
Curva de fusão
As substâncias, de uma forma geral, aumentam de volume quando sofrem fusão e ao contrário diminuem de volume quando se solidificam. Como consequência, um aumento na pressão acarreta um aumento no ponto de fusão (temperatura de fusão).
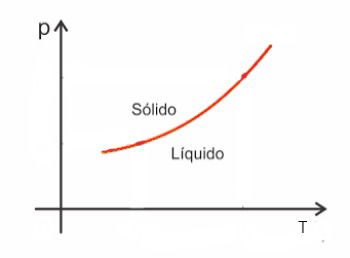
Contudo, existem algumas exceções dentre elas a água, que na fusão diminuem de volume. Neste caso, um aumento na pressão acarreta uma diminuição no ponto de fusão.
Assim, a curva de fusão dessas substâncias terá o seguinte aspecto:
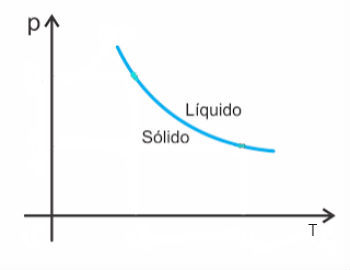
Exemplo
Considere o diagrama de fases do CO2 (dióxido de carbono) representado abaixo e responda as questões:
a) Qual a fase o CO2 , quando a sua temperatura for de - 60 ºC e a pressão de 50 atm?
b) Uma certa quantidade de CO2 líquido é submetida a uma pressão de 56 atm, e está confinada em um recipiente. Se o líquido for aquecido, mantendo-se a pressão constante, qual o valor da temperatura em que irá ocorrer a vaporização?
c) Qual o valor da temperatura e da pressão do ponto triplo do CO2?
d) Uma pedra de gelo seco (CO2) está submetida a uma pressão de 2 atm. Ela é aquecida, mantendo-se a pressão constante. Em um determinado instante começa a ocorre uma mudança de fase. Qual o nome desta mudança?
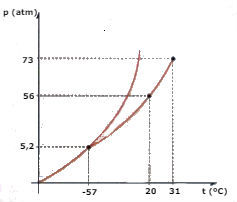
Resolução:
a) Observando o diagrama, concluímos que o CO2 estará na fase sólida.
b) Irá ocorrer a vaporização quando a temperatura atingir 20 ºC.
c) O ponto triplo corresponde a interseção das três curvas, no caso do CO2, quando apresenta uma temperatura de - 57 ºC e pressão de 5,2 atm, os três estados físicos podem coexistir.
d) Irá ocorrer a sublimação
Exercícios Resolvidos
1) Enem - 2000
Ainda hoje, é muito comum as pessoas utilizarem vasilhames de barro (moringas ou potes de cerâmica não esmaltada) para conservar água a uma temperatura menor do que a do ambiente. Isso ocorre porque:
a) o barro isola a água do ambiente, mantendo-a sempre a uma temperatura menor que a dele, como se fosse isopor.
b) o barro tem poder de “gelar” a água pela sua composição química. Na reação, a água perde calor.
c) o barro é poroso, permitindo que a água passe através dele. Parte dessa água evapora, tomando calor da moringa e do restante da água, que são assim resfriadas.
d) o barro é poroso, permitindo que a água se deposite na parte de fora da moringa. A água de fora sempre está a uma temperatura maior que a de dentro.
e) a moringa é uma espécie de geladeira natural, liberando substâncias higroscópicas que diminuem naturalmente a temperatura da água.
2) Ita - 2013
Considere o diagrama de fase hipotético representado esquematicamente na figura a seguir:
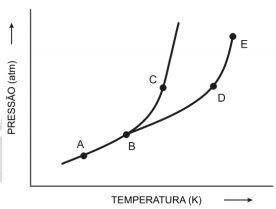
O que representam os pontos A, B, C, D e E?
3) UECE - 2009
Observando o diagrama de fase PT mostrado a seguir. Pode-se concluir, corretamente, que uma substância que passou pelo processo de sublimação segue a trajetória:
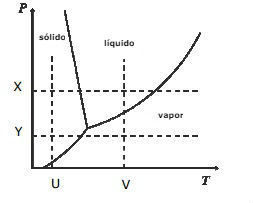
a) X ou Y
b) Y ou U
c) U ou V
d) V ou X
Continue praticando com
exercícios sobre diagramas de fases (com gabarito explicado)
exercícios sobre transformações da matéria (com gabarito comentado).
GOUVEIA, Rosimar. Diagrama de Fases. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/diagrama-de-fases/. Acesso em:

