Evaporação
Evaporação é a passagem do estado líquido para o estado gasoso. Ela ocorre na superfície livre dos líquidos, de forma lenta e gradual, em qualquer temperatura.
Uma substância quando está no estado líquido apresenta menor força de coesão entre seus átomos do que quando está no estado sólido.
Nesse estado, as moléculas estão mais afastadas, em constante agitação e se movimentam no interior do líquido com diferentes velocidades.
Desta forma, as partículas com maior velocidade, ao atingirem a superfície livre do líquido, conseguem escapar passando para o estado gasoso.

Velocidade da Evaporação
Existem fatores que influenciam na velocidade com que ocorre a evaporação, são eles:
- Temperatura: quanto maior a temperatura, maior será a velocidade da evaporação. Pois quanto maior a temperatura, maior é a energia cinética das partículas. Desta forma, mais partículas irão escapar da superfície do líquido.
- Natureza do líquido: existem substâncias que evaporam mais facilmente, elas são chamadas de substâncias voláteis. O éter, o álcool e a acetona são exemplos de substâncias voláteis.
- Área da superfície livre: como a evaporação ocorre na superfície livre dos líquidos, quanto maior a superfície, maior é a quantidade de partículas que deixará o líquido.
- Concentração de vapor sobre o líquido: quanto maior a quantidade de vapor, menor será a velocidade de evaporação.
- Pressão exercida sobre o líquido: quanto maior a pressão, menor é a velocidade de evaporação.
Diferença entre Evaporação e Ebulição
Tanto a evaporação quanto a ebulição representam a mudança do estado líquido para o estado gasoso. Contudo, enquanto a evaporação ocorre de maneira gradual, a ebulição acontece de forma rápida.
Para que ocorra a ebulição, é necessário que o líquido atinja, para uma dada pressão, uma determinada temperatura, chamada de ponto de ebulição. Já a evaporação pode ocorrer em qualquer temperatura.
Separação de Misturas
A cristalização fracionada é um processo separação de misturas heterogêneas. Ela é usada quando as substâncias que formam a mistura estão no estado sólido.
Neste processo é adicionado a mistura um líquido que dissolva todos os componentes sólidos. Os componentes então se cristalizam separadamente após a solução sofrer evaporação.
Este processo é utilizado por exemplo nas salinas para a obtenção dos sais da água do mar.

Evaporação e o Ciclo da Água
A evaporação é um dos processos que constituem o ciclo da água. A energia proveniente do Sol, aquece a superfície livre dos lagos, rios, mares e oceanos.
Este aquecimento faz com que uma parte da água evapore, passando para o estado de vapor. Este, ao atingir as camadas mais altas da atmosfera, se resfriam e se condensam formando as nuvens.
Ao ocorrer a precipitação, a água volta para a superfície na forma líquida, infiltrando no solo e formando os lençóis subterrâneos.
Parte dessa água é absorvida pelas plantas, que devolvem a atmosfera pela transpiração o vapor da água.
Mudanças de fase
A mudança do estado líquido para o estado gasoso é chamada genericamente de vaporização, pois engloba, além da evaporação, outros dois processos: ebulição e calefação.
Existem ainda outros processos de mudança de estado. São eles:
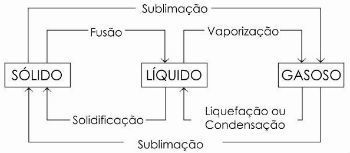
No diagrama abaixo representamos os três estados físicos da matéria e as respectivas mudanças de estado:
Saiba mais:
GOUVEIA, Rosimar. Evaporação. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/evaporacao/. Acesso em:

