Sublimação
A sublimação é a mudança do estado sólido para o estado gasoso e vice-versa, sem passar pelo estado líquido.
Para uma substância sofrer o processo de sublimação é necessário que esteja submetida a determinados valores de temperatura e pressão.
A naftalina e o CO2 sólido (gelo-seco) são exemplos de substâncias que sofrem sublimação nas condições ambientes.

Diagrama de fases
Podemos descobrir o estado físico de uma substância conhecendo os valores da temperatura e da pressão que ela está submetida.
Para isso, utilizamos diagramas construídos para cada substância, a partir de valores encontrados experimentalmente.
Chamado de "diagrama de fases", ele está dividido em três regiões que representam os estados sólido, líquido e gasoso. As linhas que delimitam essas regiões sinalizam os pontos no qual a substância muda de fase.
O ponto triplo do diagrama indica a temperatura e a pressão em que pode coexistir a substância nas três fases. Abaixo desse ponto se localiza a curva de sublimação.
O pontos nesta curva determinam os valores de pressão e temperatura em que ocorrerá a sublimação.
Quando um sólido está submetido a uma pressão menor que a do ponto triplo, se ele for aquecido irá passar diretamente para o estado gasoso.
A mudança do estado sólido direto para o estado gasoso, também pode acontecer pela diminuição da pressão quando sua temperatura é menor que a do ponto triplo.
Saiba mais em: Mudanças de Estado Físico.
Diagrama de fases do Dióxido de carbono (CO2 )
O ponto triplo do CO2 ocorre quando a pressão é de 5 atm. Este fato justifica ser comum vemos a ocorrência da sublimação no gelo-seco, visto que a pressão ambiente é de 1 atmosfera.
Por esta razão, não se obtém dióxido de carbono líquido em condições ambientes. Nestas condições, ele está ou no estado sólido ou no estado de vapor.
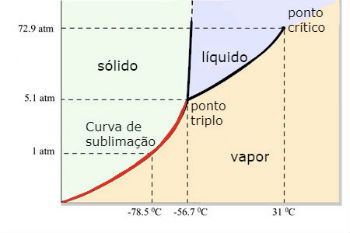
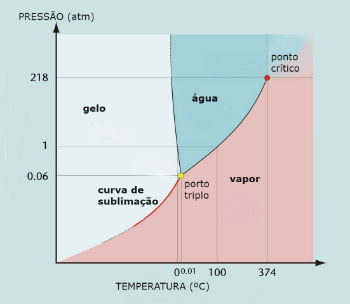
Diagrama de fases da água (H2O)
O ponto triplo da água ocorre quando a pressão é de apenas 0,06 atm. Assim, em condições ambientes não é comum ocorrer a sublimação da água.
Para saber mais, leia também:
- Estados Físicos da água
- Estados Físicos da Matéria
- Liquefação ou Condensação
- Propriedades da Matéria
- Solidificação
- Fusão
- Vaporização
- Ebulição
- Evaporação
GOUVEIA, Rosimar. Sublimação. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/sublimacao/. Acesso em:

