Exercícios de termoquímica para o ENEM (com gabarito explicado)
A termoquímica estuda as trocas de energia que acompanham as reações químicas, especialmente na forma de calor, permitindo compreender processos como combustão, neutralização e energia dos alimentos.
Nesta lista de exercícios, você vai aplicar conceitos como entalpia, Lei de Hess e energia de ligação em situações contextualizadas. As questões apresentam resolução comentada passo a passo para reforçar o aprendizado e facilitar a revisão do conteúdo.
Questão 1
A queima de combustíveis fósseis é a principal fonte de energia utilizada pela sociedade moderna. A gasolina, por exemplo, é uma mistura de hidrocarbonetos, sendo o octano (C₈H₁₈) um de seus principais componentes. A combustão completa do octano pode ser representada pela seguinte equação termoquímica:
C₈H₁₈(l) + 25/2 O₂(g) → 8 CO₂(g) + 9 H₂O(l) ΔH = -5470 kJ/mol
Um automóvel consome 5,7 kg de octano em uma viagem. Considerando a massa molar do octano = 114 g/mol e que toda a energia liberada na combustão seja aproveitada, a quantidade total de energia liberada nesse processo é de aproximadamente:
a) 5,47 × 10⁴ kJ
b) 1,37 × 10⁵ kJ
c) 2,74 × 10⁵ kJ
d) 5,47 × 10⁵ kJ
Resposta: alternativa C
Resolução passo a passo:
Massa de octano: 5,7 kg = 5700 g
Número de mols de octano: n = 5700 g / 114 g/mol = 50 mols
Energia liberada por mol: 5470 kJ/mol
Energia total liberada: 50 mol × 5470 kJ/mol = 273.500 kJ = 2,735 × 10⁵ kJ
Portanto, a energia liberada é de aproximadamente 2,74 × 10⁵ kJ.
Questão 2
O gráfico abaixo representa o perfil energético de uma reação química genérica A + B → C + D, mostrando a variação de entalpia (ΔH) e a energia de ativação (Ea).
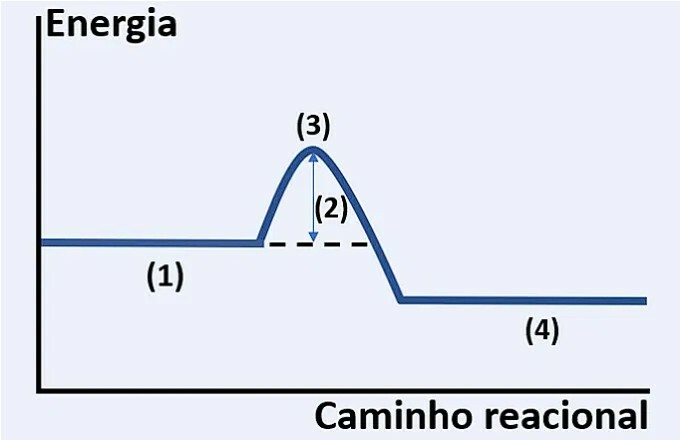
a) A reação representada é endotérmica, pois a entalpia dos produtos é menor que a dos reagentes.
b) A energia de ativação da reação direta é a diferença energética entre o complexo ativado e os produtos.
c) A adição de um catalisador diminuiria a energia de ativação (Ea), mas não alteraria o valor de ΔH.
d) A reação inversa (C + D → A + B) apresenta a mesma energia de ativação que a reação direta.
Resposta: alternativa C
Vamos analisar cada alternativa:
A: Incorreta. Se a entalpia dos produtos é menor que a dos reagentes, o ΔH é negativo, caracterizando uma reação exotérmica. O gráfico mostra produtos com energia menor que os reagentes, indicando reação exotérmica.
B: Incorreta. A energia de ativação (Ea) é a diferença de energia entre os reagentes e o complexo ativado (pico da curva), não entre o complexo ativado e os produtos.
C: Correta. Um catalisador aumenta a velocidade da reação ao diminuir a energia de ativação (Ea), fornecendo um caminho alternativo de menor energia. No entanto, o catalisador não altera a entalpia (ΔH), pois não interfere nas energias dos reagentes e produtos.
D: Incorreta. A reação inversa (endotérmica, neste caso) possui uma energia de ativação maior que a da reação direta, pois os produtos da reação direta estão em nível energético mais baixo.
Questão 3
As reações químicas podem ser classificadas como exotérmicas ou endotérmicas dependendo da variação de entalpia envolvida. A tabela abaixo apresenta os valores aproximados de entalpia de formação (ΔH°f) de algumas substâncias a 25°C e 1 atm:
| Substância | ΔH°f (kJ/mol) |
| CH₄(g) | -74,8 |
| CO₂(g) | -393,5 |
| H₂O(l) | -285,8 |
| O₂(g) | 0 |
Considere a reação de combustão completa do metano: CH₄(g) + 2 O₂(g) → CO₂(g) + 2 H₂O(l).
Com base nos dados fornecidos, a variação de entalpia (ΔH°) dessa reação e sua classificação são, respectivamente:
a) -890,4 kJ/mol; exotérmica
b) -890,4 kJ/mol; endotérmica
c) +890,4 kJ/mol; exotérmica
d) +890,4 kJ/mol; endotérmica
Resposta: alternativa A
Resolução utilizando a Lei de Hess:
ΔH° = Σ ΔH°f(produtos) – Σ ΔH°f(reagentes)
Produtos: CO₂(g) + 2 H₂O(l) → (-393,5) + 2 × (-285,8) = -393,5 – 571,6 = -965,1 kJ
Reagentes: CH₄(g) + 2 O₂(g) → (-74,8) + 2 × 0 = -74,8 kJ
ΔH° = (-965,1) – (-74,8) = -965,1 + 74,8 = -890,3 kJ/mol (aproximadamente -890,4 kJ/mol)
Como ΔH° é negativo, a reação é exotérmica.
Questão 4
O ácido clorídrico concentrado (HCl) reage com hidróxido de sódio sólido (NaOH) em uma reação de neutralização que libera grande quantidade de calor. Em um experimento, um estudante dissolveu 4,0 g de NaOH(s) em 100 mL de água e, em seguida, adicionou 100 mL de uma solução de HCl 1,0 mol/L. A temperatura da mistura aumentou de 25,0°C para 31,5°C. Considere que o calor específico da solução resultante é 4,18 J·g⁻¹·°C⁻¹ e que a densidade da solução é 1,0 g/mL. A capacidade calorífica do calorímetro é desprezível.
Com base nesses dados, o calor liberado na reação de neutralização (em kJ) é aproximadamente:
a) 1,09 kJ
b) 2,18 kJ
c) 5,43 kJ
d) 10,9 kJ
Resposta: alternativa C
Resolução passo a passo:
Massa total da solução: Volume final = 100 mL + 100 mL = 200 mL. Densidade = 1,0 g/mL → m = 200 g.
Variação de temperatura: ΔT = 31,5°C – 25,0°C = 6,5°C.
Quantidade de calor absorvido pela solução (Q): Q = m × c × ΔT = 200 g × 4,18 J·g⁻¹·°C⁻¹ × 6,5°C = 200 × 4,18 × 6,5 = 5434 J = 5,434 kJ.
Calor liberado pela reação: Como o calor foi absorvido pela solução, a reação liberou a mesma quantidade de calor (em módulo): ≈ 5,43 kJ.
Observação: O enunciado fornece 4,0 g de NaOH e 100 mL de HCl 1,0 mol/L. Pode-se verificar que ambos estão em proporção estequiométrica (0,1 mol de cada), portanto o calor calculado corresponde à neutralização de 0,1 mol de ácido e base.
Questão 5
A energia armazenada nos alimentos é medida em quilocalorias (kcal) ou quilojoules (kJ). A tabela abaixo apresenta a composição aproximada de um sanduíche e os valores energéticos de cada macronutriente:
| Macronutriente | Massa (g) |
Energia (kcal/g) |
| Carboidrato | 40 | 4,0 |
| Proteína | 20 | 4,0 |
| Gordura | 15 | 9,0 |
Considere que 1 cal = 4,18 J e que o corpo humano aproveita integralmente a energia química dos alimentos. A energia total disponível nesse sanduíche, em quilojoules (kJ), é de aproximadamente:
a) 255 kJ
b) 617 kJ
c) 940 kJ
d) 1568 kJ
Resposta: alternativa D.
Energia proveniente dos carboidratos: 40 g × 4,0 kcal/g = 160 kcal
Energia proveniente das proteínas: 20 g × 4,0 kcal/g = 80 kcal
Energia proveniente das gorduras: 15 g × 9,0 kcal/g = 135 kcal
Energia total em kcal: 160 + 80 + 135 = 375 kcal
Conversão para kJ: 375 kcal × 4,18 kJ/kcal = 1567,5 kJ
Questão 6
A reação de combustão do etanol (C₂H₅OH) é utilizada em motores de veículos e também em experimentos de termoquímica. Considere as seguintes equações termoquímicas:
I. C₂H₅OH(l) + 3 O₂(g) → 2 CO₂(g) + 3 H₂O(l) ΔH₁ = -1367 kJ/mol
II. C(grafite) + O₂(g) → CO₂(g) ΔH₂ = -393,5 kJ/mol
III. H₂(g) + ½ O₂(g) → H₂O(l) ΔH₃ = -285,8 kJ/mol
Com base na Lei de Hess, a entalpia de formação do etanol (2 C(grafite) + 3 H₂(g) + ½ O₂(g) → C₂H₅OH(l)) é, em kJ/mol:
a) +277,7
b) -277,7
c) +823,5
d) -823,5
Resposta: alternativa A
Resolução utilizando a Lei de Hess:
Para obter a reação de formação do etanol, devemos manipular as equações dadas de modo que tenhamos o etanol do lado dos produtos em quantidade correspondente a 1mol:
Inverter a equação I: 2 CO₂(g) + 3 H₂O(l) → C₂H₅OH(l) + 3 O₂(g) ΔH = +1367 kJ
Manter a equação II multiplicada por 2: 2 C(grafite) + 2 O₂(g) → 2 CO₂(g) ΔH = 2 × (-393,5) = -787 kJ
Manter a equação III multiplicada por 3: 3 H₂(g) + ³/₂ O₂(g) → 3 H₂O(l) ΔH = 3 × (-285,8) = -857,4 kJ
Somando as três equações:
2 CO₂(g) + 3 H₂O(l) + 2 C(grafite) + 2 O₂(g) + 3 H₂(g) + ³/₂ O₂(g) → C₂H₅OH(l) + 3 O₂(g) + 2 CO₂(g) + 3 H₂O(l)
Cancelando 2 CO₂(g), 3 H₂O(l) e 3 O₂(g) (reagentes e produtos), obtemos:
2 C(grafite) + 3 H₂(g) + ½ O₂(g) → C₂H₅OH(l) (pois 2 O₂ + ³/₂ O₂ = 3,5 O₂; subtraindo 3 O₂ do produto, restam ½ O₂ nos reagentes)
Somando os ΔH: ΔH = (+1367) + (-787) + (-857,4) = 1367 – 787 – 857,4 = 1367 – 1644,4 = -277,4 kJ (aproximadamente -277,7 kJ). Portanto, a entalpia de formação do etanol é negativa. A alternativa correta é B.
Questão 7
Os aerossóis utilizados em desodorantes e outros produtos continham, no passado, gases CFCs (clorofluorcarbonetos) que, ao atingirem a estratosfera, catalisavam a decomposição do ozônio (O₃). Atualmente, esses gases foram substituídos por hidrocarbonetos como o propano e o butano. O calor de combustão do propano (C₃H₈) é de -2220 kJ/mol, e do butano (C₄H₁₀) é de -2877 kJ/mol.
Considere que um frasco de desodorante aerosol contém 88 g de propano. A energia liberada na combustão completa dessa quantidade de propano é, aproximadamente:
a) 1110 kJ
b) 2220 kJ
c) 3330 kJ
d) 4440 kJ
Resposta: alternativa D.
Resolução passo a passo:
Massa molar do propano (C₃H₈): 3 × 12 + 8 × 1 = 36 + 8 = 44 g/mol.
Número de mols em 44 g: n = 88 g / 44 g/mol = 2 mol.
Calor de combustão: ΔH = -2220 kJ/mol (libera 2220 kJ por mol).
Energia liberada: 2 mol × 2220 kJ/mol = 4440 kJ.
Portanto, a energia liberada é de aproximadamente 4440 kJ.
Questão 8
A entalpia de ligação é definida como a energia necessária para romper 1 mol de uma determinada ligação química no estado gasoso. A tabela abaixo apresenta valores aproximados de entalpias de ligação (kJ/mol):
| Ligação | Entalpia (kJ/mol) |
| H-H | 436 |
| Cl-Cl | 243 |
| H-Cl | 431 |
Considere a reação: H₂(g) + Cl₂(g) → 2 HCl(g).
Utilizando os dados da tabela, a variação de entalpia (ΔH) dessa reação é de:
a) -183 kJ/mol
b) +183 kJ/mol
c) -366 kJ/mol
d) +366 kJ/mol
Resposta: alternativa A
Resolução utilizando entalpias de ligação:
ΔH = Σ (energia absorvida para quebrar ligações nos reagentes) – Σ (energia liberada na formação de ligações nos produtos)
Ligações quebradas nos reagentes: 1 mol de H-H (436 kJ) + 1 mol de Cl-Cl (243 kJ) = 679 kJ (absorvido)
Ligações formadas nos produtos: 2 mols de H-Cl (2 × 431 = 862 kJ) (liberado, portanto negativo no cálculo)
ΔH = 679 – 862 = -183 kJ/mol
O sinal negativo indica que a reação é exotérmica.
Para estudar mais: Termoquímica: o que é, reações químicas e entalpia
Faça mais questões de termoquímica com gabarito explicado.
ALVES, Gustavo. Exercícios de termoquímica para o ENEM (com gabarito explicado). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/exercicios-de-termoquimica-para-o-enem-com-gabarito-explicado/. Acesso em:

