Solução-Tampão
A solução-tampão é uma solução que mesmo com a adição de um ácido ou base, não sofre variação de pH. Ou seja, a solução tamponada é resistente às variações de pH.
Geralmente, são soluções compostas de um ácido fraco e um sal correspondente a esse ácido. Ou ainda, uma base fraca e um sal correspondente a essa base.
O que é pH?
Lembre-se que o pH (potencial hidrogeniônico) define o caráter básico ou ácido de uma solução.
Na escala de pH uma solução neutra (ou água pura) possui um pH de 7. Abaixo disso, são consideradas as soluções ácidas. Por outro lado, as que estão acima do pH 7 são chamadas de solução básicas.
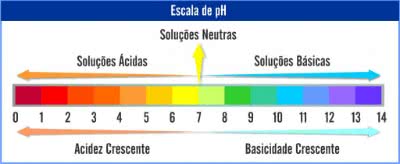
Representação da escala de pH
Além do pH, temos o pOH que significa potencial hidroxiliônico. No entanto, a escala de pH é mais usada.
Leia também:
O Sangue e a Solução-Tampão
Um bom exemplo de solução tamponada é o nosso sangue. As trocas gasosas que ele realiza (transporte de oxigênio e gás carbônico) só acontecem porque o sangue está tamponado com pH em torno de 7,3 a 7,5.
Quando há variação de pH, o equilíbrio químico se desloca o que pode provocar acidose sanguínea (sangue mais ácido) ou alcalose sanguínea (sangue mais básico). Em ambos os casos, uma variação de 0,4 no pH sanguíneo pode levar a morte da pessoa.
Dito isso, podemos concluir que o sangue é a solução-tampão vital de todos os seres humanos.
Além do sangue, vale lembrar que todos os fluidos do nosso corpo estão sob a solução-tampão. O suco gástrico, um líquido produzido no estômago, também é tamponado com um pH que varia entre 1,6 e 1,8.
Exercícios de Vestibular com Gabarito
1. (UFMG) Considere duas soluções aquosas líquidas, I e II, ambas de pH = 5,0. A solução é tampão e a solução II não.
Um béquer contém 100 mL da solução I e um segundo béquer contém 100 mL da solução II. A cada umas dessas soluções, adicionam-se 10 mL de NaOH aquoso concentrado.
Assinale a alternativa que apresenta corretamente as variações de pH das soluções I e II, após a adição de NaOH (aq).
a) O pH de ambas irá diminuir e o pH de I será maior do que o de II.
b) O pH de ambas irá aumentar e o pH de I será igual ao de II.
c) O pH de ambas irá diminuir e o pH de I será igual ao de II.
d) O pH de ambas irá aumentar e o pH de I será menor do que o de II.
2. (Mackenzie-SP) O pH do sangue de um indivíduo, numa situação de tranquilidade, é igual a 7,5. Quando esse indivíduo se submete a exercícios físicos muito fortes, ocorre a hiperventilação. Na hiperventilação, a respiração, ora acelerada, retira muito CO2 do sangue, podendo até provocar tontura. Admita que no sangue ocorra o equilíbrio:
CO2 + H2O ↔ HCO-3 + H+
Em situação de hiperventilação, a concentração de H+ no sangue e o pH do sangue tendem respectivamente:
| [H+] | pH | |
|---|---|---|
| a) | a aumentar | a ser menor que 7,5 |
| b) | a diminuir | a ser maior que 7,5 |
| c) | a manter-se inalterada | a ser maior que 7,5 |
| d) | a aumentar | a ser maior que 7,5 |
| e) | a diminuir | a ser menor que 7,5 |
3. (FEI-SP) Dissolvendo-se acetato de sódio numa solução de ácido acético, a constante de ionização do ácido, o grau de ionização do ácido e o pH da solução, respectivamente:
a) diminui; não se altera; diminui
b) não se altera; diminui; aumenta
c) aumenta; diminui; não se altera
d) não se altera; aumenta; diminui
e) não se altera; aumenta; não se altera
Solução-Tampão. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/solucao-tampao/. Acesso em:
