Terceira Lei da Termodinâmica: o que é, entropia e zero absoluto
A Terceira Lei da Termodinâmica trata do comportamento da matéria com entropia aproximada a zero.
De acordo com essa lei, sempre que um sistema encontra-se em equilíbrio termodinâmico, a sua entropia aproxima-se de zero.
A segunda lei da termodinâmica relaciona-se com a entropia. Na sequência, a terceira lei surge como uma tentativa de estabelecer um ponto de referência absoluto que determine a entropia.
Walther Nernst (1864-1941) foi o físico que se ocupou dos princípios que serviram de base para a terceira lei da termodinâmica.
De acordo com Nernst, a entropia teria a tendência de apresentar um valor mínimo caso a temperatura de uma substância pura fosse igual ou aproximada a zero absoluto.
Para tanto, Nernst propôs a fórmula abaixo, a qual mostra que a variação da entropia (ΔS) e a temperatura (T) tendem a valores mínimos, ou seja, 0:
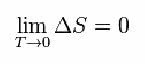
Mas, o que é Entropia?
Entropia é a forma como as moléculas se organizam no sistema. Essa organização se traduz em desordem, não no sentido de confusão, mas sim no sentido de movimentação e agitação de moléculas.
Quanto mais as moléculas podem se movimentar, mais desorganizadas elas são, mais entropia elas têm.
Inicialmente, Nernst sugeriu que a entropia proposta por ele seria possível somente em cristais perfeitos.
Por fim, concluiu que a temperatura igual a zero absoluto não existia, fazendo da terceira lei uma lei polêmica.
Desta forma, para muitos físicos, não se trata de uma lei, mas sim de uma regra.
Passados tantos anos (desde 1912), os cientistas tentam obter essa temperatura ou temperaturas que se aproximem cada vez mais do zero absoluto. Assim, descobriram que ela somente é possível em gases, descartando qualquer substância em estado sólido ou líquido.
Leia também:
- Lei Zero da Termodinâmica
- Primeira Lei da Termodinâmica
- Segunda Lei da Termodinâmica
- Exercícios sobre Termodinâmica
Terceira Lei da Termodinâmica: o que é, entropia e zero absoluto. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/terceira-lei-da-termodinamica/. Acesso em:

