Autocatálise: o que é, como funciona e exemplos
Autocatálise é um processo químico no qual um dos produtos da reação atua como catalisador para a própria reação. Ou seja, a reação começa lentamente, mas, assim que uma pequena quantidade de produto é formada, ela passa a "ajudar" a transformar mais reagentes, acelerando o processo de forma crescente.
Imagine uma reação química que, à medida que produz seus resultados, cria as ferramentas necessárias para que ela própria aconteça mais rapidamente. Esse fenômeno, que desafia a intuição de que a causa sempre vem antes do efeito, é conhecido como autocatálise.
Em termos gráficos, podemos chegar a uma representação como esta a seguir:
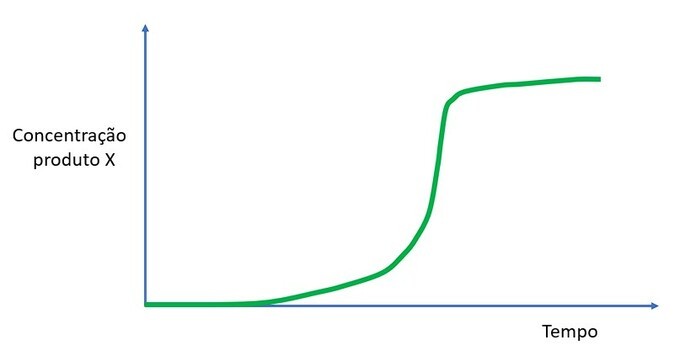
Veja que a concentração de um produto X aumenta pouco no início da reação. Assim, há pouco catalisador para acelerar a reação e formar mais produto. À medida que X vai se formando e vai catalisando a reação, mais rápida a reação fica até ter X suficiente para formar subitamente uma grande quantidade do produto. Quando toda a quantidade máxima de produto é formada, não há mais alteração na concentração do produto X e, assim, a velocidade volta a cair.
Como funciona o mecanismo autocatalítico
Para entender a mágica da autocatálise, vamos compará-la com uma obra de construção. Na catálise comum, é como se um pedreiro experiente (o catalisador externo) fosse chamado para ajudar a construir uma parede. Ele acelera o serviço, mas não faz parte da parede em si.
Já na autocatálise, é como se o primeiro tijolo colocado na parede (o produto) atraísse magneticamente os outros tijolos (reagentes) para se encaixarem perfeitamente ao seu redor. Quanto mais tijolos são colocados, mais forte fica o campo magnético e mais rápida fica a construção.
Em termos químicos, o mecanismo geralmente segue um padrão:
-
Iniciação Lenta: No início, a reação ocorre de forma espontânea, mas muito devagar, transformando uma quantidade ínfima de reagente (A) em produto (B). Essa é a fase de "indução".
Exemplo: A → B (lento)
-
Ação Catalítica: O produto (B) formado começa a interagir com o restante do reagente (A), formando um complexo intermediário que facilita e acelera a transformação de A em mais B.
Exemplo: A + B → 2B (rápido)
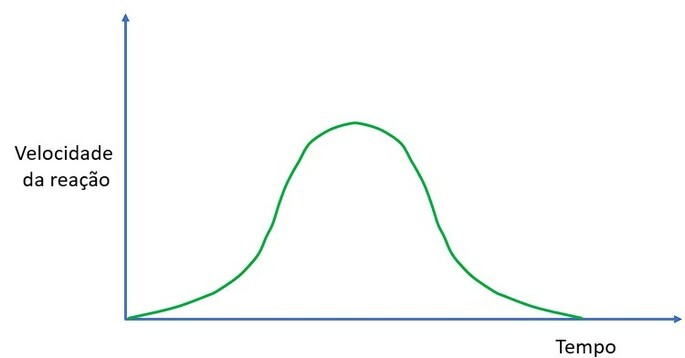
Observe que, na segunda etapa, o produto B é consumido e regenerado, mas o resultado final é a conversão de A em B de forma muito mais eficiente. Esse é um ciclo de retroalimentação positiva: quanto mais B é produzido, mais ele acelera a produção de ainda mais B. A velocidade da reação aumenta exponencialmente até que os reagentes comecem a se esgotar. Neste momento, por ter pouco reagente, a velocidade volta a cair até se tornar nula:
Exemplos concretos de autocatálise
A autocatálise não é apenas um conceito teórico; ela está presente em diversos processos químicos e biológicos fundamentais.
1. A Reação do Relógio de Iodo (Iodato e Ácido Sulfuroso)
Um dos exemplos mais clássicos e visualmente impressionantes é a reação entre iodato de potássio (KIO₃) e ácido sulfuroso (H₂SO₃). Inicialmente, a solução permanece incolor. Lentamente, íons iodeto (I⁻) são formados.
Quando a concentração desses íons atinge um ponto crítico, eles começam a catalisar sua própria produção a partir do iodato, num ciclo que leva a um aumento explosivo na concentração de iodo molecular (I₂), que reage com o amido presente na solução, fazendo-a mudar subitamente para um azul profundo. É como se a reação "decidisse" acontecer toda de uma vez.
2. Reação de Oxidação do Ácido Oxálico pelo Permanganato
Nesta reação, o permanganato de potássio (KMnO₄), de cor roxa, oxida o ácido oxálico (H₂C₂O₄). O manganês no permanganato (Mn⁺⁷) é reduzido a manganês (Mn⁺²), que é incolor.
O que torna o processo autocatalítico é que os íons Mn⁺² produzidos atuam como catalisadores para a redução do restante do Mn⁺⁷. No início, a descoloração do roxo é lenta, mas, à medida que Mn⁺² se acumula, a reação se acelera, e a solução se torna incolor cada vez mais rapidamente.
3. Replicação de DNA (ou RNA)
Em um nível mais fundamental, a própria replicação do material genético pode ser vista como um processo autocatalítico. Uma molécula de DNA (o "produto") serve como molde para a criação de uma nova molécula de DNA (cópia).
As enzimas envolvidas (como a DNA polimerase) são catalisadores externos, mas a informação e a estrutura que guiam a criação da nova molécula vêm da própria molécula de DNA existente. Em certos modelos de origem da vida, acredita-se que moléculas de RNA autocatalíticas (ribozimas) tenham sido capazes de se replicar sem a ajuda de proteínas.
Diferenciação entre catálise comum e autocatálise
Para fixar o conceito, a tabela abaixo resume as principais diferenças entre a catálise "comum" e a autocatálise.
| Característica | Catálise comum | Autocatálise |
|---|---|---|
| Catalisador | Externo | Produto da reação |
| Velocidade | Velocidade constante | Velocidade tem um "pico" |
| Perfil | Concentração do produto aumenta quase linearmente | Concentração aumenta de maneira sigmoidal |
| Analogia | Uma fábrica que liga as máquinas (catalisador) para produzir um carro (produto). | O primeiro carro produzido (produto) é projetado para rebocar os materiais e construir os próximos carros mais rápido. |
Veja também: Exercícios de química para o 2º ano do Ensino Médio (com gabarito explicado)
Referências Bibliográficas
BOUDART, M. Kinetics of chemical processes. Englewood Cliffs: Prentice-Hall, 1968
CHORKENDORFF, I.; NIEMANTSVERDRIET, J. W. Concepts of modern catalysis and kinetics. 2. ed., rev. and enl. Weinheim: Wiley-VCH, 2007
FROMENT, Gilbert F.; BISCHOFF, Kenneth B.; DE WILDE, Juray. Chemical reactor analysis and design. 3. ed. Hoboken: John Wiley & Sons, 2011.
ALVES, Gustavo. Autocatálise: o que é, como funciona e exemplos. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/autocatalise-o-que-e-como-funciona-e-exemplos/. Acesso em:


