Lista de Exercícios sobre Química Orgânica (de Enem)
Questão 1
Um microempresário do ramo de cosméticos utiliza óleos essenciais e quer produzir um creme com fragrância de rosas. O principal componente do óleo de rosas tem cadeia poli-insaturada e hidroxila em carbono terminal. O catálogo dos óleos essenciais apresenta, para escolha da essência, estas estruturas químicas:
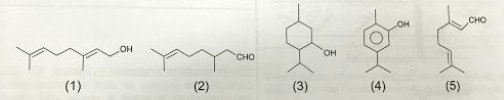
Qual substância o empresário deverá utilizar?
1
2
3
4
5
Fonte: Questão 94 da prova azul do segundo dia do Enem 2020
Questão 2
A enorme quantidade de resíduos gerados pelo consumo crescente da sociedade traz para a humanidade uma preocupação socioambiental, em especial pela quantidade de lixo produzido. Além da reciclagem e do reúso, pode-se melhorar ainda mais a qualidade de vida, substituindo polímeros convencionais por polímeros biodegradáveis. Esses polímeros têm grandes vantagens socioambientais em relação aos convencionais porque
não são tóxicos.
não precisam ser reciclados.
não causam poluição ambiental quando descartados.
são degradados em um tempo bastante menor que os convencionais.
apresentam propriedades mecânicas semelhantes aos convencionais.
Fonte: Questão 92 da prova azul do segundo dia do Enem 2020
Questão 3
A composição de um dos refrigerantes mais ácidos mundialmente consumido é mantida em segredo pelos seus produtores. Existe uma grande especulação em torno da “fórmula” dessa bebida, a qual envolve algumas das seguintes substâncias:
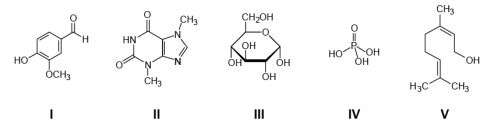
A substância presente nesse refrigerante, responsável pelo seu acentuado caráter ácido, é a
I
II
III
IV
V
Fonte: Questão 128 da prova azul do segundo dia do Enem 2020 Digital
Questão 4
Os feromônios de insetos são substâncias responsáveis pela comunicação química entre esses indivíduos. A extração de feromônios para uso agronômico no lugar de pesticidas convencionais geralmente é inviável, pois são encontrados em baixa concentração nas glândulas de armazenamento. Uma das formas de solucionar essa limitação é a síntese em laboratório dos próprios feromônios ou de isômeros que apresentem a mesma atividade. Suponha que o composto apresentado seja um feromônio natural e que seu tautômero seja um potencial substituto.
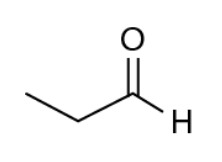
Com base na estrutura química desse feromônio, seu potencial substituto é representado pela substância:
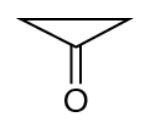
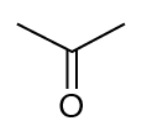
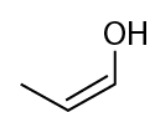
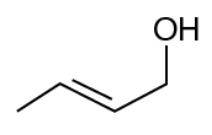
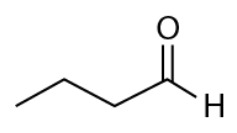
Fonte: Questão 101 da prova azul do segundo dia do Enem 2020 Digital
Questão 5
O propranolol é um fármaco pouco solúvel em água utilizado no tratamento de algumas doenças cardiovasculares. Quando essa substância é tratada com uma quantidade estequiométrica de um ácido de Brönsted-Lowry, o grupamento de maior basicidade reage com o próton, levando à formação de um derivado solúvel em água.
GONSALVES, A. A. et al. Contextualizando reações ácido-base de acordo com a teoria protônica de Brönsted-Lowry usando comprimidos de propranolol e nimesulida. Química Nova, n. 8, 2013 (adaptado).
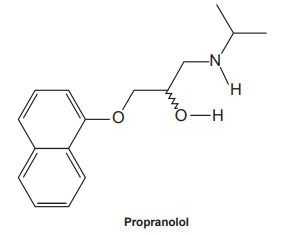
O ácido de Brönsted-Lowry reage com
a hidroxila alcoólica.
os anéis aromáticos.
as metilas terminais.
o grupamento amina.
o oxigênio do grupamento éter.
Fonte: Enem 2020
Questão 6
Uma lagarta ao comer as folhas do milho, induz no vegetal a produção de óleos voláteis cujas estruturas estão mostradas a seguir:
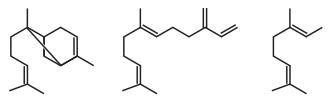
A volatilidade desses óleos é decorrência do(a)
elevado caráter covalente.
alta miscibilidade em água.
baixa estabilidade química.
grande superfície de contato.
fraca interação intermolecular.
Fonte: ENEM PPL - 2020
Questão 7
Grandes reservatórios de óleo leve de melhor qualidade e que produz petróleo mais fino foram descobertos no litoral brasileiro numa camada denominada pré-sal, formada há 150 milhões de anos. A utilização desse recurso energético acarreta para o ambiente um desequilíbrio no ciclo do
nitrogênio, devido à nitrificação ambiental transformando amônia em nitrito.
nitrogênio, devido ao aumento dos compostos nitrogenados no ambiente terrestre.
carbono, devido ao aumento dos carbonatos dissolvidos no ambiente marinho.
carbono, devido à liberação das cadeias carbônicas aprisionadas abaixo dos sedimentos.
fósforo, devido à liberação dos fosfatos acumulados no ambiente marinho.
Fonte: Questão 97 da prova azul do segundo dia do Enem 2020
Questão 8
No processo de industrialização da mamona, além do óleo que contém vários ácidos graxos, é obtida uma massa orgânica, conhecida como torta de mamona. Esta massa tem potencial para ser utilizada como fertilizante para o solo e como complemento em rações animais devido a seu elevado valor proteico. No entanto, a torta apresenta compostos tóxicos e alergênicos diferentemente do óleo da mamona. Para que a torta possa ser utilizada na alimentação animal, é necessário um processo de descontaminação.
Revista Química Nova na Escola. V. 32, no1, 2010 (adaptado)A característica presente nas substâncias tóxicas e alergênicas, que inviabiliza sua solubilização no óleo de mamona, é a
lipofilia.
hidrofilia.
hipocromia.
cromatofilia.
hiperpolarização.
Fonte: Questão 55 da prova azul do primeiro dia do Enem 2011
Questão 9
O senso comum nos diz que os polímeros orgânicos (plásticos) em geral são isolantes elétricos. Entretanto, os polímeros condutores são materiais orgânicos que conduzem eletricidade. O que faz estes polímeros diferentes é a presença das ligações covalentes duplas conjugadas com ligações simples, ao longo de toda a cadeia principal, incluindo grupos aromáticos. Isso permite que um átomo de carbono desfaça a ligação dupla com um vizinho e refaça-a com outro. Assim, a carga elétrica desloca-se dentro do material.
De acordo com o texto, qual dos polímeros seguintes seria condutor de eletricidade?
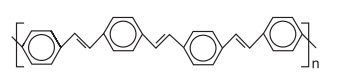
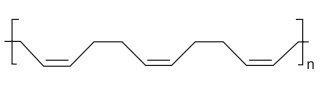
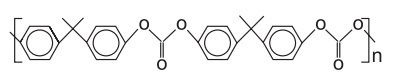
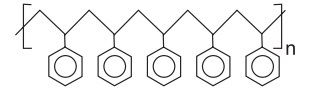
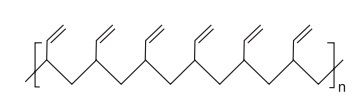
Fonte: Questão 50 da prova cinza do primeiro dia do Enem 2012 Segunda Aplicação
Questão 10
Pesticidas são substâncias utilizadas para promover o controle de pragas. No entanto, após sua aplicação em ambientes abertos, alguns pesticidas organoclorados são arrastados pela água até lagos e rios e, ao passar pelas guelras dos peixes, podem difundir-se para seus tecidos lipídicos e lá se acumularem.
A característica desses compostos, responsável pelo processo descrito no texto, é o(a)
baixa polaridade.
baixa massa molecular.
ocorrência de halogênios.
tamanho pequeno das moléculas.
presença de hidroxilas nas cadeias.
Fonte: Questão 80 da prova azul do primeiro dia do Enem 2015
Questão 12
O citral, substância de odor fortemente cítrico, é obtido a partir de algumas plantas como o capim-limão, cujo óleo essencial possui aproximadamente 80%, em massa, da substância. Uma de suas aplicações é na fabricação de produtos que atraem abelhas, especialmente do gênero Apis, pois seu cheiro é semelhante a um dos feromônios liberados por elas. Sua fórmula molecular é C10H16O, com uma cadeia alifática de oito carbonos, duas insaturações, nos carbonos 2 e 6; e dois grupos substituintes metila, nos carbonos 3 e 7. O citral possui dois isômeros geométricos, sendo o trans o que mais contribui para o forte odor.
Para que se consiga atrair um maior número de abelhas para uma determinada região, a molécula que deve estar presente em alta concentração no produto a ser utilizado é:
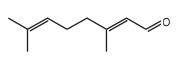
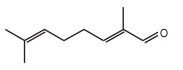
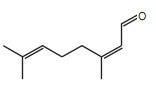
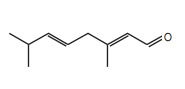
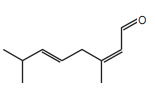
Fonte: Questão 58 da prova azul do primeiro dia do Enem 2013
Questão 13
O uso de embalagens plásticas descartáveis vem crescendo em todo o mundo, juntamente com o problema ambiental gerado por seu descarte inapropriado. O politereftalato de etileno (PET), cuja estrutura é mostrada, tem sido muito utilizado na indústria de refrigerantes e pode ser reciclado e reutilizado. Uma das opções possíveis envolve a produção de matérias-primas, como o etilenoglicol (1,2-etanodiol), a partir de objetos compostos de PET pós-consumo.
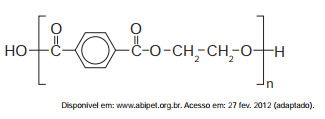
Com base nas informações do texto, uma alternativa para a obtenção de etilenoglicol a partir do PET é a
solubilização dos objetos.
combustão dos objetos.
trituração dos objetos.
hidrólise dos objetos.
fusão dos objetos.
Fonte: Questão 54 da prova azul do primeiro dia do Enem 2013
Questão 14
As fraldas descartáveis que contêm o polímero poliacrilato de sódio (1) são mais eficientes na retenção de água que as fraldas de pano convencionais, constituídas de fibras de celulose (2).
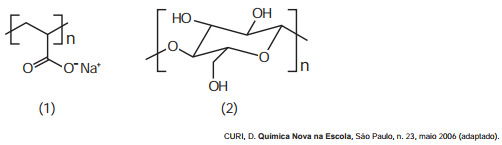
A maior eficiência dessas fraldas descartáveis, em relação às de pano, deve-se às
interações dipolo-dipolo mais fortes entre o poliacrilato e a água, em relação às ligações de hidrogênio entre a celulose e as moléculas de água.
interações íon-íon mais fortes entre o poliacrilato e as moléculas de água, em relação às ligações de hidrogênio entre a celulose e as moléculas de água.
ligações de hidrogênio mais fortes entre o poliacrilato e a água, em relação às interações íon-dipolo entre a celulose e as moléculas de água.
ligações de hidrogênio mais fortes entre o poliacrilato e as moléculas de água, em relação às interações dipolo induzido-dipolo induzido entre a celulose e as moléculas de água.
interações íon-dipolo mais fortes entre o poliacrilato e as moléculas de água, em relação às ligações de hidrogênio entre a celulose e as moléculas de água.
Fonte: Questão 86 da prova azul do primeiro dia do Enem 2013
Questão 15
A produção mundial de alimentos poderia se reduzir a 40% da atual sem a aplicação de controle sobre as pragas agrícolas. Por outro lado, o uso frequente dos agrotóxicos pode causar contaminação em solos, águas superficiais e subterrâneas, atmosfera e alimentos. Os biopesticidas, tais como a piretrina e a coronopilina, têm sido uma alternativa na diminuição dos prejuízos econômicos, sociais e ambientais gerados pelos agrotóxicos.
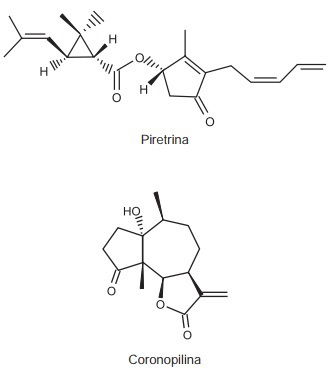
Identifique as funções orgânicas presentes simultaneamente nas estruturas dos dois biopesticidas apresentados:
Éter e éster.
Cetona e éster.
Álcool e cetona.
Aldeído e cetona.
Éter e ácido carboxílico.
Fonte: Questão 49 da prova azul do primeiro dia do Enem 2012
Questão 16
Em uma planície, ocorreu um acidente ambiental em decorrência do derramamento de grande quantidade de um hidrocarboneto que se apresenta na forma pastosa à temperatura ambiente. Um químico ambiental utilizou uma quantidade apropriada de uma solução de para-dodecil-benzenossulfonato de sódio, um agente tensoativo sintético, para diminuir os impactos desse acidente. Essa intervenção produz resultados positivos para o ambiente porque
promove uma reação de substituição no hidrocarboneto, tornando-o menos letal ao ambiente.
a hidrólise do para-dodecil-benzenossulfonato de sódio produz energia térmica suficiente para vaporizar o hidrocarboneto.
a mistura desses reagentes provoca a combustão do hidrocarboneto, o que diminui a quantidade dessa substância na natureza.
a solução de para-dodecil-benzenossulfonato possibilita a solubilização do hidrocarboneto.
o reagente adicionado provoca uma solidificação do hidrocarboneto, o que facilita sua retirada do ambiente.
Fonte: Questão 70 da prova azul do primeiro dia do Enem 2012
Questão 17
A talidomida é um sedativo leve e foi muito utilizado no tratamento de náuseas, comuns no início da gravidez. Quando foi lançada, era considerada segura para o uso de grávidas, sendo administrada como uma mistura racêmica composta pelos seus dois enantiômeros (R e S). Entretanto, não se sabia, na época, que o enantiômero S leva à malformação congênita, afetando principalmente o desenvolvimento normal dos braços e pernas do bebê.
Essa malformação congênita ocorre porque esses enantiômeros
reagem entre si.
não podem ser separados.
não estão presentes em partes iguais.
interagem de maneira distinta com o organismo.
são estruturas com diferentes grupos funcionais.
Fonte: Questão 52 da prova azul do primeiro dia do Enem 2014
Questão 18
Com o objetivo de substituir as sacolas de polietileno, alguns supermercados têm utilizado um novo tipo de plástico ecológico, que apresenta em sua composição amido de milho e uma resina polimérica termoplástica, obtida a partir de uma fonte petroquímica.
Nesses plásticos, a fragmentação da resina polimérica é facilitada porque os carboidratos presentes
dissolvem-se na água.
absorvem água com facilidade.
caramelizam por aquecimento e quebram.
são digeridos por organismos decompositores.
decompõem-se espontaneamente em contato com água e gás carbônico.
Fonte: Questão 78 da prova azul do primeiro dia do Enem 2014
Lista de Exercícios sobre Química Orgânica (de Enem). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/lista-de-exercicios-sobre-quimica-organica-de-enem/. Acesso em:
