Destilação fracionada: o que é, processo e exemplos
A destilação fracionada é um processo utilizado para separar misturas homogêneas formadas por pelo menos dois líquidos miscíveis. A separação por esse método baseia-se nos diferentes pontos de ebulição dos componentes da mistura.
Esse tipo de separação é geralmente aplicado a misturas que apresentam componentes com cerca de 25 ºC de diferença do ponto de ebulição.
O principal aparelho para o processo é a coluna de fracionamento, também chamada de coluna de destilação, que apresenta em seu interior uma série de obstáculos para impedir que todos os componentes da mistura volatilizem ao mesmo tempo.
Basicamente, aquece-se a mistura em um balão de destilação até que haja mudança de estado físico do componente de menor ponto de ebulição. Em seguida, o vapor passa por uma coluna fracionada, que separa as frações, e após isso o condensador faz a substância voltar ao estado líquido para que seja direcionada ao recipiente de coleta.
A destilação fracionada é muito utilizada em indústrias e laboratórios, tendo um grande significado comercial. São exemplos de aplicações: purificação da água, separação de componentes de petróleo e separação do ar liquefeito.
O petróleo, por exemplo, é uma mistura de hidrocarbonetos, como butano (PE 20 ºC), gasolina (PE 150 ºC) e querosene (PE 300 ºC). Por isso, a ordem de separação dos componentes na destilação fracionada do menor ao maior ponto de ebulição é: butano, gasolina e querosene.
Equipamentos da destilação fracionada
Na destilação fracionada é utilizado um sistema composto pelas seguintes peças:
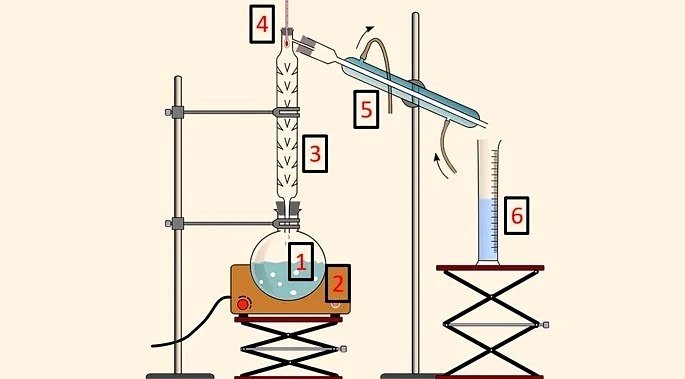
- Balão de destilação (1), que contém a mistura;
- Manta aquecedora (2), que fornece calor à mistura;
- Coluna de destilação (3), que permite a separação de acordo com a temperatura;
- Termômetro (4), para acompanhar a mudança de temperatura;
- Condensador (5), para resfriar o componente evaporado;
- Proveta (6), para recolher o componente separado no estado líquido.
Processo de separação na destilação fracionada
Primeiramente, a mistura é colocada no balão de destilação junto com os grânulos anti-colisão para evitar que ocorra uma evaporação rápida.
A coluna fracionada é conectada ao balão de destilação. À medida que a mistura é aquecida, o vapor sobe para a coluna, cujo interior é revestido com "obstáculos", geralmente de contas de vidro ou porcelana.
O contato do fluido no interior da coluna faz com que as substâncias da mistura ao passarem pelo equipamento percam calor e apenas o componente de menor ponto de ebulição segue ao topo da coluna.
O vapor que atinge o condensador é então resfriado até que haja a liquefação, ou seja, retorne para o estado líquido e seja recolhido no frasco receptor.
Leia também: O que é destilação?
Destilação fracionada do petróleo
O petróleo é uma mistura complexa de compostos orgânicos e os diferentes componentes separados no processo de destilação são chamados de frações. As frações do petróleo são formadas por hidrocarbonetos, como gasolina, diesel, querosene e betume.
A separação das frações é feita na torre de destilação, uma coluna de aço preenchida com bandejas que possuem "obstáculos" para passagem do petróleo.
Inicialmente, o petróleo é aquecido em uma fornalha e a mistura aquecida é alimentada no fundo de uma torre de destilação. A temperatura da torre é maior na parte inferior e menor no seu topo para impedir que as frações mais pesadas sejam evaporadas com os componentes mais leves.
Os hidrocarbonetos de maior cadeia carbônica são condensados e removidos na parte inferior da torre. Essas frações são escuras, viscosas e mais difíceis de evaporar. Já os de cadeia simples, têm pontos de ebulição mais baixos e, por isso, condensam em temperaturas mais próximas do topo da torre, onde são recolhidos.
Saiba mais sobre refino do petróleo.
Diferença entre destilação simples e fracionada
A destilação simples é aplicada quando queremos separar um sólido dissolvido em um líquido. Para isso, aquecemos a mistura até que o solvente evapore. Esse processo é mais rápido e requer menos energia que a destilação fracionada.
Um exemplo de mistura que pode ser separada por destilação simples é água e sal. A água por ter um ponto de ebulição muito inferior ao sal de cozinha é evaporada quando se aquece a mistura e após passar por um condensador, é recolhida em outro recipiente.
A destilação fracionada é aplicada à separação de líquidos miscíveis entre si, como água e acetona.
Para praticar: Exercícios sobre destilação (com gabaritos explicados)
Adquira mais conhecimento com os conteúdos:
Destilação simples e fracionada
Referências Bibliográficas
BROWN, T. L.; LEMAY JR., H. E.; BURSTEN, B. E.; BURDGE, J. R. Química a ciência central. 9ª ed. Pearson Prentice Hall do Brasil, 2008.
USBERCO, J.; SALVADOR, E. Química Geral. 12ª.ed. São Paulo: Saraiva, 2006.
RUSSEL. J. B. Química Geral. vol. 1. Makron, 1996.
BATISTA, Carolina. Destilação fracionada: o que é, processo e exemplos. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/destilacao-fracionada/. Acesso em:

