Exercícios de química para o 2º ano do Ensino Médio (com gabarito explicado)
Os conteúdos de Química do 2º ano do Ensino Médio aprofundam temas como termoquímica, equilíbrio químico, eletroquímica e cinética. Para auxiliar na revisão, reunimos exercícios com gabarito explicado que exploram cálculos, interpretação de gráficos e aplicação das principais leis químicas. As questões combinam teoria e prática, preparando você para avaliações e vestibulares. Resolva as atividades e consolide seus conhecimentos!
Questão 1
Considere a equação termoquímica para a combustão completa do metano:
CH₄(g) + 2 O₂(g) → CO₂(g) + 2 H₂O(l) ΔH = -890 kJ/mol
Com base nessa informação, analise as afirmativas abaixo e assinale a alternativa CORRETA:
I. A reação é exotérmica, liberando 890 kJ por mol de metano queimado.
II. Se a água formada estiver no estado gasoso (vapor), o valor absoluto do ΔH será menor que 890 kJ.
III. A entalpia dos produtos (CO₂ + 2 H₂O) é maior que a entalpia dos reagentes (CH₄ + 2 O₂).
IV. Para a combustão de 32 g de metano (massa molar = 16 g/mol), a energia liberada será de 1780 kJ.
a) Apenas I e II estão corretas.
b) Apenas I, II e IV estão corretas.
c) Apenas II e III estão corretas.
d) Todas as afirmativas estão corretas.
Resposta: alternativa B.
Vamos analisar cada afirmativa:
I. Correta. ΔH negativo indica reação exotérmica (libera calor).
II. Correta. Se a água formar vapor, parte da energia liberada será usada para vaporizar a água (calor latente), resultando em ΔH menos negativo (ex: -802 kJ/mol).
III. Incorreta. Em reação exotérmica, a entalpia dos produtos é menor que a dos reagentes. A diferença (negativa) é a energia liberada.
IV. Correta. 32 g de CH₄ correspondem a 2 mols (16 g/mol × 2). Energia liberada = 2 mol × 890 kJ/mol = 1780 kJ.
Portanto, estão corretas I, II e IV.
Questão 2
A entalpia de formação do monóxido de carbono (CO) não pode ser medida diretamente, pois a combustão do carbono tende a formar CO₂. Utilizando a Lei de Hess, considere as seguintes equações termoquímicas:
I. C(grafite) + O₂(g) → CO₂(g) ΔH₁ = -393,5 kJ
II. CO(g) + ½ O₂(g) → CO₂(g) ΔH₂ = -283,0 kJ
Com base nessas informações, a entalpia de formação do CO (C(grafite) + ½ O₂(g) → CO(g)) é:
a) -110,5 kJ
b) -55,25 kJ
c) +110,5 kJ
d) -676,5 kJ
Resposta: alternativa A.
Pela Lei de Hess, podemos manipular as equações para obter a reação desejada:
Mantemos a equação I: C(grafite) + O₂(g) → CO₂(g) ΔH₁ = -393,5 kJ
Invertemos a equação II: CO₂(g) → CO(g) + ½ O₂(g) ΔH = +283,0 kJ (inverter inverte o sinal)
Somamos as duas equações:
C(grafite) + O₂(g) + CO₂(g) → CO₂(g) + CO(g) + ½ O₂(g)
Cancelando CO₂ e O₂ (1 - ½ = ½), obtemos:
C(grafite) + ½ O₂(g) → CO(g)
Somando os ΔH: ΔH = (-393,5) + (+283,0) = -110,5 kJ.
Portanto, a entalpia de formação do CO é -110,5 kJ/mol.
Questão 3
A decomposição da água oxigenada (peróxido de hidrogênio, H₂O₂) é uma reação lenta em condições normais, mas pode ser acelerada pela adição de dióxido de manganês (MnO₂). Sobre esse processo, assinale a alternativa CORRETA:
a) O MnO₂ atua como reagente, sendo consumido durante a reação para formar novos produtos.
b) O MnO₂ aumenta a energia de ativação da reação, tornando-a mais rápida.
c) O MnO₂ é um catalisador que diminui a energia de ativação, aumentando a velocidade da reação sem ser consumido.
d) O MnO₂ desloca o equilíbrio da reação para o lado dos produtos, aumentando o rendimento.
Resposta: alternativa C.
A: O MnO₂ atua como catalisador na decomposição do H₂O₂ (2 H₂O₂ → 2 H₂O + O₂). Catalisadores:
B: Diminuem a energia de ativação da reação, permitindo que mais moléculas tenham energia suficiente para reagir.
C: Aumentam a velocidade da reação, mas não são consumidos no processo (regeneram-se ao final).
D: Não alteram o equilíbrio químico nem o rendimento da reação, apenas aceleram sua obtenção.
Questão 4
Considere o seguinte equilíbrio químico, estabelecido em um recipiente fechado a uma dada temperatura:
N₂(g) + 3 H₂(g) ⇌ 2 NH₃(g)
Em um experimento, as concentrações no equilíbrio foram medidas: [N₂] = 0,5 mol/L, [H₂] = 1,5 mol/L e [NH₃] = 1,0 mol/L. O valor da constante de equilíbrio (Kc) para essa reação, na temperatura do experimento, é aproximadamente:
a) 0,15
b) 0,30
c) 1,33
d) 0,59
Resposta: alternativa D.
A expressão da constante de equilíbrio Kc para a reação é:
Substituindo os valores na fórmula e calculando Kc:
Questão 5
Uma pilha eletroquímica é construída com base nas seguintes semirreações e seus respectivos potenciais padrão de redução (E°red):
Ag⁺(aq) + e⁻ → Ag(s) E° = +0,80 V
Zn²⁺(aq) + 2 e⁻ → Zn(s) E° = -0,76 V
Sobre essa pilha, assinale a alternativa CORRETA:
a) O eletrodo de zinco atua como cátodo, sofrendo redução.
b) A diferença de potencial (ddp) padrão da pilha é de 0,04 V.
c) Os elétrons fluem, pelo circuito externo, do eletrodo de prata para o eletrodo de zinco.
d) A reação global da pilha é: Zn(s) + 2 Ag⁺(aq) → Zn²⁺(aq) + 2 Ag(s).
Resposta: alternativa D.
Vamos analisar:
O eletrodo com maior potencial de redução (Ag: +0,80 V) sofre redução e é o cátodo (polo positivo).
O eletrodo com menor potencial de redução (Zn: -0,76 V) sofre oxidação e é o ânodo (polo negativo).
A: Incorreta. O zinco é o ânodo (oxidação).
B: Incorreta. ΔE° = E°red (maior) - E°red (menor) = 0,80 - (-0,76) = 1,56 V.
C: Incorreta. Os elétrons fluem do ânodo (Zn, onde ocorre oxidação) para o cátodo (Ag, onde ocorre redução).
D: Correta. Oxidação do Zn: Zn → Zn²⁺ + 2 e⁻; Redução do Ag⁺: 2 Ag⁺ + 2 e⁻ → 2 Ag. Somando: Zn(s) + 2 Ag⁺(aq) → Zn²⁺(aq) + 2 Ag(s).
Questão 6
O metanol (CH₃OH) é um combustível líquido que pode ser utilizado em células a combustível. Considere as seguintes equações termoquímicas:
I. C(grafite) + O₂(g) → CO₂(g) ΔH = -393,5 kJ/mol
II. H₂(g) + ½ O₂(g) → H₂O(l) ΔH = -285,8 kJ/mol
III. CH₃OH(l) + ³/₂ O₂(g) → CO₂(g) + 2 H₂O(l) ΔH = -726,4 kJ/mol
Com base nessas informações, a entalpia de formação do metanol (C(grafite) + 2 H₂(g) + ½ O₂(g) → CH₃OH(l)) é, em kJ/mol:
a) -238,7
b) +238,7
c) -1405,7
d) +1405,7
Resposta: alternativa A.
Pela Lei de Hess, devemos manipular as equações para obter a reação desejada:
Mantemos a equação I:
C(grafite) + O₂(g) → CO₂(g) ΔH₁ = -393,5 kJ
Multiplicamos a equação II por 2:
2 H₂(g) + O₂(g) → 2 H₂O(l) ΔH₂ = 2 × (-285,8) = -571,6 kJ
Invertemos a equação III:
CO₂(g) + 2 H₂O(l) → CH₃OH(l) + ³/₂ O₂(g) ΔH₃ = +726,4 kJ (inverte o sinal)
Somando as três equações:
C(grafite) + O₂(g) + 2 H₂(g) + O₂(g) + CO₂(g) + 2 H₂O(l) → CO₂(g) + 2 H₂O(l) + CH₃OH(l) + ³/₂ O₂(g)
Cancelando CO₂, 2 H₂O(l) e simplificando os oxigênios (O₂ + O₂ = 2 O₂ nos reagentes; ³/₂ O₂ nos produtos; restam ½ O₂ nos reagentes), obtemos exatamente a reação desejada.
Somando os ΔH: ΔH = (-393,5) + (-571,6) + (+726,4) = -238,7 kJ/mol.
Questão 7
Considere o gráfico abaixo que representa o perfil de uma reação química genérica: A + B → C + D.
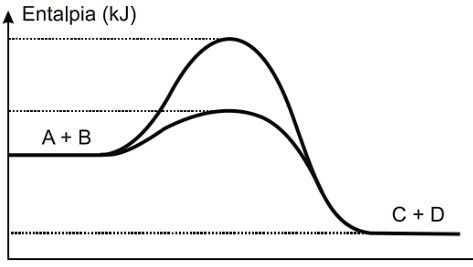
Analisando o gráfico, que mostra a energia ao longo do caminho da reação, assinale a alternativa CORRETA:
a) A reação é endotérmica, pois a energia dos produtos é maior que a dos reagentes.
b) A energia de ativação da reação direta é a diferença de energia entre os reagentes e o complexo ativado.
c) A adição de um catalisador aumentaria a energia de ativação, tornando a reação mais lenta.
d) As duas curvas apresentam mesma energia de ativação.
Resposta: alternativa B.
Analisando cada alternativa:
A: Incorreta. O gráfico mostra produtos com energia menor que a dos reagentes → reação exotérmica.
B: Correta. A energia de ativação (Eat) é a diferença de energia entre o complexo ativado (pico das curvas) e a energia dos reagentes.
C: Incorreta. Catalisadores diminuem a energia de ativação, acelerando a reação.
D: Incorreta. Como as curvas têm picos em alturas diferentes, as energias de ativação também são diferentes.
Questão 8
Considere o seguinte equilíbrio químico, estabelecido em um recipiente fechado:
2 NO₂(g) (castanho) ⇌ N₂O₄(g) (incolor) ΔH < 0 (exotérmica)
Um recipiente contém uma mistura desses gases em equilíbrio, apresentando coloração castanha intermediária. Assinale a alternativa que descreve CORRETAMENTE o que ocorre com o sistema quando se aumenta a temperatura do recipiente:
a) O equilíbrio se desloca para a direita, formando mais N₂O₄ incolor, e a coloração castanha diminui.
b) O equilíbrio se desloca para a esquerda, formando mais NO₂ castanho, e a coloração castanha se intensifica.
c) A constante de equilíbrio (Kc) aumenta, favorecendo a formação de N₂O₄.
d) Não há alteração na coloração, pois a temperatura não afeta equilíbrios gasosos.
Resposta: alternativa B.
Pelo Princípio de Le Chatelier, o aumento de temperatura favorece a reação endotérmica, que absorve o calor adicional.
A reação direta (2 NO₂ → N₂O₄) é exotérmica (ΔH < 0).
Portanto, a reação inversa (N₂O₄ → 2 NO₂) é endotérmica.
Ao aquecer, o equilíbrio se desloca para a esquerda (sentido endotérmico), consumindo N₂O₄ incolor e produzindo mais NO₂ castanho.
Consequência: a coloração castanha se intensifica e a constante Kc diminui.
Questão 9
A eletrólise ígnea do cloreto de sódio (NaCl) fundido é um processo industrial importante para a obtenção de sódio metálico e gás cloro. Nesse processo, os íons Na⁺ e Cl⁻ estão livres no estado líquido (fundido). Sobre a eletrólise ígnea do NaCl, assinale a alternativa CORRETA:
a) No cátodo (polo negativo), ocorre a oxidação dos íons cloreto (Cl⁻), formando gás cloro (Cl₂).
b) No ânodo (polo positivo), ocorre a redução dos íons sódio (Na⁺), formando sódio metálico (Na).
c) Os íons Na⁺ migram para o cátodo, onde sofrem redução: Na⁺ + e⁻ → Na(l).
d) A reação global da eletrólise é: 2 NaCl(l) → 2 Na(s) + Cl₂(g), que é um processo espontâneo.
Resposta: alternativa C.
Analisando cada alternativa:
A: Incorreta. No cátodo (polo negativo) ocorre redução. Quem sofre redução são os cátions (Na⁺). A oxidação dos Cl⁻ ocorre no ânodo.
B: Incorreta. No ânodo (polo positivo) ocorre oxidação. Quem sofre oxidação são os ânions (Cl⁻). A redução dos Na⁺ ocorre no cátodo.
C: Correta. Íons positivos (cátions) migram para o cátodo (eletrodo negativo), onde recebem elétrons e sofrem redução: Na⁺ + e⁻ → Na(l).
D: Incorreta. A reação global está correta, mas a eletrólise é um processo não espontâneo, que requer o fornecimento de energia elétrica para ocorrer.
Veja também:
Exercícios de química para o 1º ano do Ensino Médio (com gabarito explicado)
Exercícios de química para o 3º ano do Ensino Médio (com gabarito explicado)
ALVES, Gustavo. Exercícios de química para o 2º ano do Ensino Médio (com gabarito explicado). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/exercicios-de-quimica-para-o-2-ano-do-ensino-medio-com-gabarito-explicado/. Acesso em:


