Química no Enem
A Química, junto com Biologia e Física, faz parte da área de Ciências da Natureza e suas Tecnologias.
Ao todo são 45 questões, divididas entre as três disciplinas, que são aplicadas no segundo dia de prova junto com Matemática e suas Tecnologias.
Os ramos da Química que mais são explorados no Enem são: Química Geral, Físico-química, Química Orgânica e Química Ambiental.
Os enunciados das questões são contextualizados como forma de interligar as áreas do conhecimento com assuntos do cotidiano.
Assuntos de Química que mais caem no Enem
Para ir bem na prova é preciso ler com atenção as questões, interpretar os dados e relacionar com os conceitos que você estudou.
O conteúdo de Química da prova abrange os principais compostos, suas propriedades, as funções químicas que os caracterizam e as reações que eles podem fazer.

Os cálculos são pedidos para quantificar as reações e os exemplos utilizados são questões do cotidiano; seja o processo produtivo de um composto químico relevante ou até mesmo a aplicação em outras áreas, como a datação de um fóssil.
Abaixo, descrevemos os assuntos mais cobrados e o que estudar sobre cada um deles.
Química Geral
A química geral apresenta a evolução dos estudos na área da Química, as relações qualitativas e quantitativas das reações e a introdução de conceitos e termos que são a base para entender as demais áreas.
Basicamente, essa ramo abrange os princípios da Química para entendermos a composição, propriedades e reatividade da matéria.
A Química Geral no Enem explora mais:
| Tema | Principais tópicos |
|---|---|
| Tabela periódica |
Elementos químicos e sua organização, classificação dos elementos e propriedades da matéria. |
| Propriedades periódicas | |
| Misturas | Tipos de misturas, principais métodos de separação e as frações obtidas. |
| Técnicas de separação | |
| Estequiometria | Cálculos químicos de rendimento e pureza. |
| Cálculos estequiométricos | |
| Ligações químicas | Como os átomos se ligam para formar as diversas substâncias e interação entre as moléculas. |
| Forças intermoleculares | |
| Geometria molecular | Características dos principais compostos. |
| Solubilidade |
Questão de Química Geral
(Enem/2018) Na mitologia grega, Nióbia era a filha de Tântalo, dois personagens conhecidos pelo sofrimento. O elemento químico de número atômico (Z) igual a 41 tem propriedades químicas e físicas tão parecidas com as do elemento de número atômico 73 que chegaram a ser confundidos.
Por isso, em homenagem a esses dois personagens da mitologia grega, foi conferido a esses elementos os nomes de nióbio (Z = 41) e tântalo (Z = 73). Esses dois elementos químicos adquiriram grande importância econômica na metalurgia, na produção de supercondutores e em outras aplicações na indústria de ponta, exatamente pelas propriedades químicas e físicas comuns aos dois.
KEAN, S. A colher que desaparece: e outras histórias reais de loucura, amor e morte a partir dos elementos químicos. Rio de Janeiro: Zahar, 2011 (adaptado).
A importância econômica e tecnológica desses elementos, pela similaridade de suas propriedades químicas e físicas, deve-se a
a) terem elétrons no subnível f.
b) serem elementos de transição interna.
c) pertencerem ao mesmo grupo na tabela periódica.
d) terem seus elétrons mais externos nos níveis 4 e 5, respectivamente.
e) estarem localizados na família dos alcalinos terrosos e alcalinos, respectivamente.
A resolução dessa questão necessita do conhecimento da definição de grupo (família) da Tabela Periódica.
Por isso, é muito importante ao estudar fixar os conceitos, isso te ajudará a interpretar as questões e facilitará a resolução.
Físico-química
Os sistemas tem as suas características interpretadas pelas observações das propriedades físicas e químicas.
A energia e a dinâmica das transformações químicas são estudas nesse ramo da química.

A Físico-Química no Enem explora mais:
| Tema | Principais tópicos |
|---|---|
| Soluções | Calcular a concentração de soluções (molar, comum, PPM e porcentagem). |
| Eletroquímica | Diferenciar cátodo e ânodo, comparar os potencias-padrão de redução, reações de oxidação e redução, fenômeno de corrosão, pilha e eletrólise. |
| Termoquímica | Calcular a variação de energia, conceito de entalpia de reação e lei de Hess. |
| Ácidos e bases | Calcular pH e reação de neutralização. |
| Equilíbrio químico | Conceitos gerais, constante de equilíbrio e deslocamento de equilíbrio. |
| Princípio de Le Chatelier | |
| Radioatividade | tempo de meia vida, fissão e fusão nuclear. |
Questão de Físico-química
(Enem/2009) Analise a figura.
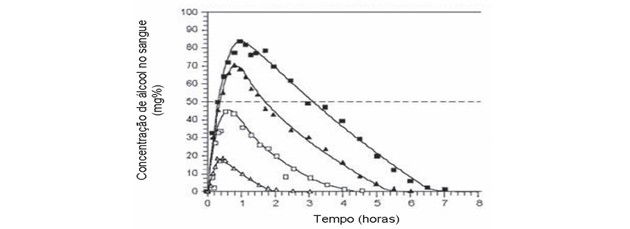
Disponível em: http//www.alcoologia.net. Acesso em: 15 jul. 2009 (adaptado).
Supondo que seja necessário dar um título para essa figura, a alternativa que melhor traduziria o processo representado seria:
a) Concentração média de álcool no sangue ao longo do dia.
b) Variação da frequência da ingestão de álcool ao longo das horas.
c) Concentração mínima de álcool no sangue a partir de diferentes dosagens.
d) Estimativa de tempo necessário para metabolizar diferentes quantidades de álcool.
e) Representação gráfica da distribuição de frequência de álcool em determinada hora do dia.
Os gráficos são uma das formas que o Enem utiliza para apresentar dados e avalia o candidato pela capacidade de interpretação. Por isso, é importante resolver as provas anteriores e se familiarizar com os tipos de questões que o exame apresenta.
Química Orgânica
Observando-se que todos os compostos de fontes vivas possuíam em sua estrutura o elemento carbono, este fato significativo levou a definição de que a Química Orgânica é o estudo dos compostos de carbono.
Ao realizar experimentos, Friedrich Wöhler conseguiu sintetizar a ureia a partir de cianato de amônio, ou seja, uma substância orgânica a partir de um composto inorgânico.
A partir de então milhões de compostos foram obtidos artificialmente a partir de reagentes minerais e por fontes mais simples de origem natural.
Devido a inúmera quantidade de compostos orgânicos, esse é um tema bastante recorrente no Enem.
A Química Orgânica no Enem explora mais:
| Tema | Principais tópicos |
|---|---|
| Carbono | Propriedades e características do carbono. |
| Funções orgânicas | Principais funções orgânicas e compostos. |
| Nomenclatura | Nomenclatura de cadeias carbônicas e classificação de carbonos. |
| Isomeria | Diferenciar estruturas orgânicas pelo tipo de isomeria. |
| Reações orgânicas | Principais reações orgânicas. |
Questão de Química Orgânica
(Enem/2014) A baunilha a uma espécie de orquídea. A partir de sua flor, a produzida a vanilina (conforme representação química), que dá origem ao aroma de baunilha.
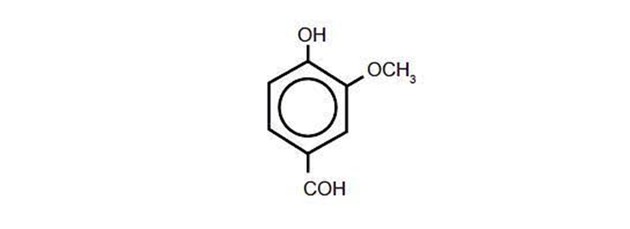
Na vanilina estão presentes as funções orgânicas
a) aldeído, éter e fenol.
b) álcool, aldeído e éter.
c) álcool, cetona e fenol.
d) aldeído, cetona e fenol.
e) ácido carboxílico, aldeído e éter.
Nessa questão foi apresentado um aroma bastante utilizado na culinária como contexto para avaliar o conhecimento de funções orgânicas.
É comum as questões relacionarem nomenclatura de compostos e pedir a sua estrutura ou vice e versa.
Por isso, é importante estudar as principais funções orgânicas e as diferenças entre elas.
Química Ambiental
Por muito tempo os avanços tecnológicos ocorreram sem a devida atenção ao meio ambiente. Com o tempo, os resultados das atividades humanas, principalmente industriais, começaram a surgir. Exemplos disso são a chuva ácida e o efeito estufa.
O conceito de Química Verde vem sendo explorado, não só como um novo caminho, mas como forma de promover a mudança de hábitos na sociedade e progresso com menos substâncias perigosas e nocivas ao meio ambiente.

A Química ambiental no Enem explora a relação entre tecnologias, sociedade e o meio ambiente.
É comum nos depararmos com questões que relatam:
| Tema | Principais tópicos |
|---|---|
| Poluição | Tipos de poluição: radioativa, do ar, da água e do solo. |
| Ciclos biogeoquímicos | Ciclo do nitrogênio e do carbono, bem como as alterações. |
| Efeito estufa | Causas, principais gases do efeito estufa e aquecimento global. |
| Chuva ácida | Causas e consequências. |
| Mudanças climáticas | Causas e consequências. |
| Combustíveis fósseis | Origem, tipos e alternativas de fontes renováveis. |
Aprofunde os seus estudos sobre Química ambiental: o que é e o que estuda (com exercícios).
Questão de Química Ambiental
(Enem/2010) Um dos grandes problemas da poluição dos mananciais (rios, córregos e outros) ocorre pelo hábito de jogar óleo utilizado em frituras nos encanamentos que estão interligados com o sistema de esgoto. Se isso ocorrer, cada 10 litros de óleo poderão contaminar 10 milhões (107) de litros de água potável.
MANUAL de etiqueta. Parte integrante das revistas Veja (ed. 2055), Cláudia (ed. 555), National Geographic (ed. 93) e Nova Escola (ed. 208) (adaptado).
Suponha que todas as famílias de uma cidade descartem os óleos de frituras através dos encanamentos e consumam 1 000 litros de óleo em frituras por semana.
Qual será, em litros, a quantidade de água potável contaminada por semana nessa cidade?
a) 102
b) 103
c) 104
d) 106
e) 109
Com esse exemplo vemos que as questões de Química Ambiental nos levam à reflexão sobre as ações do ser humano e como o meio ambiente é afetado.
Leia também:
- O que estudar para o ENEM 2025 e tirar nota 1000
- Questões de Química que caíram no Enem
- Assuntos que mais caem no Enem
Os simulados são aliados poderosos para quem está se preparando para o Enem. Confira e prepare-se melhor para o dia da prova:
Simulado de Ciências da Natureza e suas Tecnologias (ENEM 2024)
Simulado de Ciências da Natureza e suas Tecnologias (ENEM 2023)
BATISTA, Carolina. Química no Enem. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/quimica-no-enem/. Acesso em:

