Exercícios de química para o 3º ano do Ensino Médio (com gabarito explicado)
Com gabarito explicado, as questões abaixo ajudam na compreensão de reações químicas, propriedades de compostos e conceitos fundamentais. São atividades ideais para revisar conteúdos e se preparar para provas e vestibulares. Resolva e fortaleça seu aprendizado de forma prática e eficiente!
Questão 1
O benzeno (C₆H₆) é um hidrocarboneto aromático que sofre reações de substituição eletrofílica aromática. Quando o benzeno reage com ácido nítrico (HNO₃) na presença de ácido sulfúrico (H₂SO₄) concentrado, ocorre a formação de:
a) Fenol.
b) Nitrobenzeno.
c) Ácido benzoico.
d) Clorobenzeno.
Resposta: alternativa B.
A reação descrita é a nitração do benzeno, uma substituição eletrofílica aromática típica. O ácido sulfúrico atua como catalisador, gerando o eletrófilo NO₂⁺ (íon nitrônio). Esse eletrófilo ataca o anel benzênico, substituindo um átomo de hidrogênio e formando nitrobenzeno (C₆H₅-NO₂).
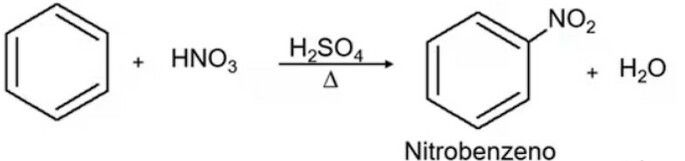
Fenol (A) seria obtido por outras vias; ácido benzoico (C) por oxidação de alquilbenzenos; clorobenzeno (D) por halogenação.
Questão 2
Dois compostos orgânicos, A e B, apresentam a mesma fórmula molecular C₃H₈O. O composto A reage com sódio metálico liberando gás hidrogênio, enquanto o composto B não reage com sódio nas mesmas condições. Com base nessas informações, assinale a alternativa que identifica CORRETAMENTE as funções orgânicas de A e B, respectivamente:
a) Álcool e éter.
b) Éter e álcool.
c) Aldeído e cetona.
d) Ácido carboxílico e éster.
Resposta: alternativa A.
A fórmula molecular C₃H₈O admite dois isômeros planos principais:
Isômero A: Álcool (propan-1-ol, CH₃-CH₂-CH₂-OH, ou propan-2-ol, CH₃-CHOH-CH₃). Álcoois possuem grupo OH e reagem com sódio liberando H₂.
Isômero B: Éter (metoxietano, CH₃-O-CH₂-CH₃). Éteres não possuem hidrogênio ligado a oxigênio e não reagem com sódio.
Portanto, A é um álcool e B é um éter.
Questão 3
A isomeria geométrica (cis-trans) é um tipo de estereoisomeria que ocorre em compostos com duplas ligações ou em estruturas cíclicas, desde que haja restrição à rotação. Qual dos seguintes compostos pode apresentar isomeria geométrica?
a) 2-metilpropano
b) 1-buteno
c) 2-buteno
d) Propeno
Resposta: alternativa C.
Para que um alceno apresente isomeria geométrica, é necessário que cada um dos dois carbonos da dupla ligação esteja ligado a dois grupos diferentes entre si.
A: 2-metilpropano: Alcano, sem dupla ligação → não apresenta.
B: 1-buteno (CH₂=CH-CH₂-CH₃): Um dos carbonos da dupla (CH₂=) tem dois hidrogênios (grupos iguais) → não apresenta.
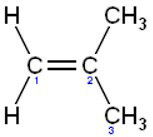
C: 2-buteno (CH₃-CH=CH-CH₃): Cada carbono da dupla está ligado a um H e a um CH₃ (grupos diferentes) → apresenta isomeria cis (grupos iguais do mesmo lado) e trans (grupos iguais em lados opostos).
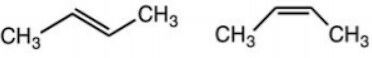
D: Propeno (CH₃-CH=CH₂): Um dos carbonos da dupla tem dois H → não apresenta.
Questão 4
A oxidação de alcenos com solução aquosa e diluída de permanganato de potássio (KMnO₄) a frio (reação de Bayer) produz:
a) Ácidos carboxílicos.
b) Cetonas e aldeídos.
c) Dióis vicinais (glicóis).
d) CO₂ e água.
Resposta: alternativa C.
A oxidação branda de alcenos com KMnO₄ diluído e frio (reação de Bayer) quebra a dupla ligação, adicionando um grupo hidroxila (-OH) a cada carbono da dupla. O produto formado são dióis vicinais (ou glicóis), compostos com duas hidroxilas em carbonos adjacentes (ex: etilenoglicol a partir do eteno).
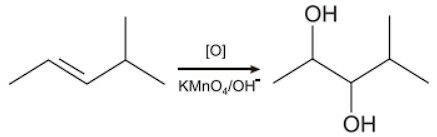
Oxidações enérgicas (com KMnO₄ concentrado e quente) quebram a molécula, produzindo cetonas, aldeídos ou ácidos carboxílicos.
Questão 5
O polietileno é um polímero de adição amplamente utilizado em embalagens plásticas.
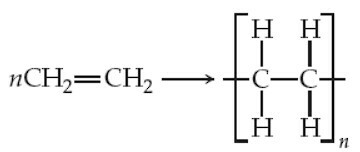
Seu monômero de partida é o:
a) Cloreto de vinila.
b) Estireno.
c) Etilenoglicol.
d) Eteno (etileno).
Resposta: alternativa D.
O polietileno é formado pela polimerização por adição do monômero eteno (CH₂=CH₂), também chamado de etileno. Milhares de unidades de eteno se ligam, abrindo a dupla ligação e formando longas cadeias (-CH₂-CH₂-)ₙ.
Cloreto de vinila (A) forma PVC; estireno (B) forma poliestireno; etilenoglicol (C) é usado na produção de polímeros de condensação (como PET).
Questão 6
A glicose (C₆H₁₂O₆) é um carboidrato fundamental no metabolismo energético dos seres vivos.
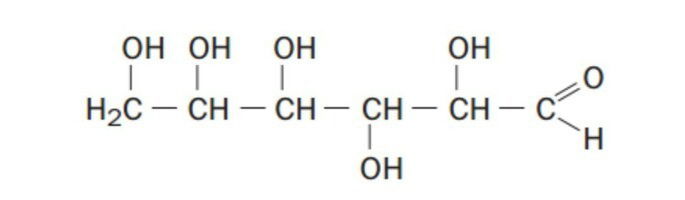
Sobre a glicose, é CORRETO afirmar que:
a) É um dissacarídeo formado pela união de frutose e galactose.
b) É um polissacarídeo de reserva energética em animais (glicogênio).
c) É um monossacarídeo do tipo aldose, com fórmula molecular C₆H₁₂O₆.
d) É encontrada apenas em vegetais, não participando do metabolismo animal.
Resposta: alternativa C.
A glicose é um monossacarídeo (não pode ser hidrolisado em unidades menores). Pertence ao grupo das aldoses (possui grupo aldeído) e tem fórmula molecular C₆H₁₂O₆.
A alternativa A descreve a lactose (dissacarídeo); B descreve o glicogênio (polissacarídeo formado por unidades de glicose, mas não é a glicose em si); D é falsa, pois a glicose é a principal fonte de energia em animais também.
Questão 7
As proteínas são macromoléculas formadas pela união de aminoácidos através de ligações peptídicas. A estrutura tridimensional funcional de uma proteína, resultante de interações entre cadeias laterais de aminoácidos distantes na sequência linear, é denominada:
a) Estrutura primária.
b) Estrutura secundária.
c) Estrutura terciária.
d) Estrutura quaternária.
Resposta: alternativa C.
Os níveis estruturais das proteínas são:
Primária: Sequência linear de aminoácidos.
Secundária: Padrões locais de dobramento (α-hélice, β-pregueada), estabilizados por pontes de hidrogênio.
Terciária: Estrutura tridimensional global, resultante de interações entre cadeias laterais de aminoácidos distantes na sequência (pontes dissulfeto, interações hidrofóbicas, pontes de H, etc.).
Quaternária: Associação de múltiplas subunidades proteicas.
A descrição corresponde à estrutura terciária.
Questão 8
O iodo-131 (¹³¹I) é um radioisótopo utilizado no tratamento de câncer de tireoide. Sua meia-vida é de 8 dias. Se uma amostra desse isótopo contém inicialmente 200 mg do material radioativo, após 32 dias a massa restante de iodo-131 será de:
a) 100 mg
b) 50 mg
c) 25 mg
d) 12,5 mg
Resposta: alternativa D.
A meia-vida (t½) é o tempo necessário para que metade dos átomos radioativos se desintegre.
Tempo total: 32 dias. Número de meias-vidas = 32 / 8 = 4 meias-vidas.
Após cada meia-vida, a massa é reduzida à metade:
Início: 200 mg
1ª meia-vida (8 dias): 100 mg
2ª meia-vida (16 dias): 50 mg
3ª meia-vida (24 dias): 25 mg
4ª meia-vida (32 dias): 12,5 mg.
Portanto, a massa restante é 12,5 mg.
Questão 9
O efeito estufa é um fenômeno natural essencial para a manutenção da vida na Terra, pois mantém a temperatura média do planeta em níveis adequados. No entanto, a intensificação desse efeito, causada por atividades humanas, tem gerado preocupações ambientais. Assinale a alternativa que apresenta APENAS gases que contribuem significativamente para o efeito estufa:
a) Oxigênio (O₂), nitrogênio (N₂) e argônio (Ar).
b) Dióxido de carbono (CO₂), metano (CH₄) e óxido nitroso (N₂O).
c) Clorofluorcarbonetos (CFCs), dióxido de enxofre (SO₂) e ozônio (O₃) troposférico.
d) Vapor dʼágua (H₂O), monóxido de carbono (CO) e hidrogênio (H₂).
Resposta: alternativa B.
Os principais gases de efeito estufa (GEE) de origem antrópica são:
Dióxido de carbono (CO₂): Queima de combustíveis fósseis e desmatamento.
Metano (CH₄): Pecuária, arrozais, aterros sanitários.
Óxido nitroso (N₂O): Uso de fertilizantes nitrogenados, queima de biomassa.
CFCs: (embora controlados pelo Protocolo de Montreal) também são GEE potentes.
Ozônio troposférico (O₃): Formado por reações fotoquímicas, é um poluente e GEE.
A alternativa A contém gases majoritários da atmosfera que não absorvem radiação infravermelha; C inclui SO₂ (principal causador de chuva ácida, não é GEE significativo); D inclui CO (tóxico, mas não é GEE significativo) e H₂.
Veja também:
Exercícios de química para o 1º ano do Ensino Médio (com gabarito explicado)
Exercícios de química para o 2º ano do Ensino Médio (com gabarito explicado)
ALVES, Gustavo. Exercícios de química para o 3º ano do Ensino Médio (com gabarito explicado). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/exercicios-de-quimica-para-o-3-ano-do-ensino-medio-com-gabarito-explicado/. Acesso em:


