Hidrólise
A hidrólise corresponde a um processo químico que envolve a quebra de uma molécula em presença de água. Lembre-se que o termo “hidro” significa água e “lise” é relativo à quebra.
Esse processo é comum na área da química (reações) e também da biologia (hidrólise de enzimas e de proteínas).
Hidrólise Salina
Na química, a hidrólise salina ocorre entre um sal e a água. Essa reação reversível produz um ácido e base correspondentes. As soluções aquosas dos ácidos possuem um pH menor que 7, e as das bases um pH maior que 7.
Os íons presentes nos sais se dissociam em presença de água e podem formam ácidos ou bases:
Sal + Água ↔ Ácido + Base
Lembre-se que o sal é sempre iônico e a água é molecular. Assim, a água se ioniza em ânions hidróxido (OH-) e cátions de hidrogênio (H+). Da mesma forma, o sal se dissocia e libera ânions e cátions.
Note que um sal de ácido forte, forma uma solução ácida:
Exemplo: H+ + H2O ↔ HOH + H+
Já um sal de base forte, forma uma solução básica:
Exemplo: OH- + H2O ↔ HOH + OH-
Um exemplo de aplicação da hidrólise salina é o do bicarbonato de sódio, o qual está presente em medicamentos que combatem a azia.
Isso ocorre porque a solução de NaHCO3 é básica, uma vez que sofreu hidrólise do ânion HCO-3:
HCO-3 + H2O ↔ H2CO3 + OH-
Grau e Constante de Hidrólise
No equilíbrio químico sempre é definido um grau e uma constante. Assim, O grau de hidrólise (α) é medido através da expressão:
![]()
Leia também: Número de Mol e Massa Molar.
A constante de hidrólise é dada pela seguinte expressão:
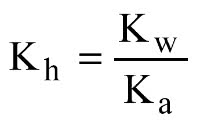
Sendo,
Kh: constante de hidrólise
Kw: produto iônico da água (aproximadamente 10-14 na temperatura ambiente)
K (a ou b): constante do ácido ou base
Considerando as seguinte reações químicas, veja abaixo um exemplo de hidrólise do NH4Cl:
NH4Cl + H2O ↔ HCl + NH4OH
NH+4 + H2O ↔ H+ + NH4OH
Sendo assim, a constante de hidrólise do NH4Cl é:
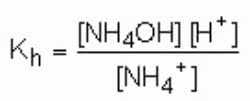
Leia mais:
Exercícios de Vestibular com Gabarito
1. (PUC-SP) Solos contendo altos teores de ferro e alumínio sob forma de íons são, em geral:
a) ácidos, devido ao fato de sofrerem oxidação.
b) ácidos, devido ao fato de sofrerem hidrólise.
c) ácidos, devido ao fato de sofrerem redução.
d) básicos, devido ao fato de sofrerem oxidação.
e) básicos, devido ao fato de sofrerem hidrólise.
2. (UFSM-RS) O caráter das soluções resultantes da hidrólise dos sais NaCl (sal de cozinha), NaHCO3 (usado como fermento) e NH4NO3 (usado na fabricação de fertilizantes) é, respectivamente:
a) neutro, básico, ácido.
b) ácido, neutro, básico
c) básico, ácido, neutro
d) neutro, básico, ácido
e) básico, neutro, básico
3. (UFU-MG) A água sanitária, utilizada no branqueamento de roupas, como bactericida e em muitas outras aplicações, é uma solução aquosa de hipoclorito de sódio (dados HClO é ácido fraco; Ka = 3,5 , 10-8). Essa solução deve:
a) ser má condutora de eletricidade, pois a maior parte do composto se encontra como moléculas não dissociadas.
b) apresentar pH = 7,0, pois se trata de um sal derivado do HCl e NaOH.
c) apresentar pH < 7,0, porque há formação de HClO, que, sendo ácido fraco, ioniza parcialmente na água, formando H+.
d) apresentar pH > 7,0, porque o ânion sofre hidrólise em água.
Hidrólise. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/hidrolise/. Acesso em:
