Exercícios sobre polímeros (com respostas explicadas)
Os polímeros estão presentes em diversos materiais do dia a dia, como plásticos, fibras, borrachas e tecidos, sendo fundamentais para a Química e para a indústria moderna.
Nestes exercícios você poderá revisar conceitos e testar seus conhecimentos sobre polímeros.
Questão 1
Polímeros são macromoléculas formadas pela repetição de uma unidade estrutural menor chamada de:
a) Isômero.
b) Monômero.
c) Oligômero.
d) Copolímero.
Resposta: alternativa B.
A definição essencial de um polímero é a de uma macromolécula composta pela repetição de muitas unidades menores e idênticas (ou similares) ligadas covalentemente. Essa unidade fundamental é o monômero. Por exemplo, o polietileno é o polímero formado pela repetição do monômero etileno (H₂C=CH₂).
Questão 2
O algodão, a lã e a seda são exemplos de polímeros classificados como:
a) Polímeros sintéticos.
b) Polímeros semissintéticos.
c) Polímeros naturais.
d) Polímeros de adição.
Resposta: alternativa C.
Polímeros naturais são aqueles produzidos por seres vivos. O algodão é formado principalmente por celulose (polímero da glicose), a lã é composta de proteínas (como a queratina), e a seda é formada pela proteína fibroína. Eles não são sintetizados pelo homem em escala industrial (sintéticos) nem modificados a partir de naturais (semissintéticos).
Questão 3
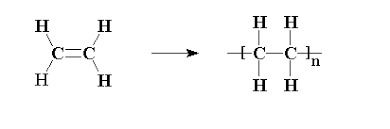
A reação que forma o polietileno a partir do etileno (CH₂=CH₂) é um exemplo clássico de polimerização por adição. Neste tipo de reação:
a) Há eliminação de uma molécula pequena (como água) a cada ligação formada entre monômeros.
b) Os monômeros se unem sem perda de átomos, através da abertura de duplas ligações.
c) Dois monômeros diferentes reagem alternadamente.
d) Ocorre apenas com monômeros que possuem grupos funcionais nas duas extremidades.
Resposta: alternativa B.
Na polimerização por adição, os monômeros insaturados (geralmente com ligações duplas ou triplas) se adicionam uns aos outros sem que nenhum subproduto seja eliminado. A reação ocorre pela quebra da ligação π (dupla) do etileno, que se transforma em duas ligações σ simples, permitindo que cada carbono se ligue a outros monômeros e forme a longa cadeia.
A alternativa A descreve a polimerização por condensação.
Questão 4
Garrafas PET e sacolas plásticas podem ser facilmente moldadas e recicladas por fusão. Essa propriedade é característica dos:
a) Polímeros termorrígidos (termofixos).
b) Polímeros termoplásticos.
c) Elastômeros vulcanizados.
d) Polímeros reticulados.
Resposta: alternativa B.
Polímeros termoplásticos possuem cadeias poliméricas lineares ou ramificadas, mantidas por forças intermoleculares (como dipolo-dipolo ou de van der Waals). Quando aquecidos, essas forças são vencidas e as cadeias deslizam umas sobre as outras, amolecendo o material e permitindo que ele seja remodelado (fundido). Após o resfriamento, solidificam novamente. Esta é a base da reciclagem mecânica.
Os termorrígidos (A) não fundem, pois possuem ligações cruzadas (reticulações) covalentes entre as cadeias.
Questão 5
O náilon e o PET (politereftalato de etileno) são exemplos de polímeros obtidos por reação de condensação. Nessa reação, é característico:
a) A necessidade de um catalisador metálico e alta pressão.
b) A formação de uma macromolécula a partir de um único tipo de monômero insaturado.
c) A eliminação de uma molécula pequena (como H₂O ou HCl) a cada ligação entre monômeros.
d) A formação de um polímero com átomos de halogênio em sua cadeia principal.
Resposta: alternativa C.
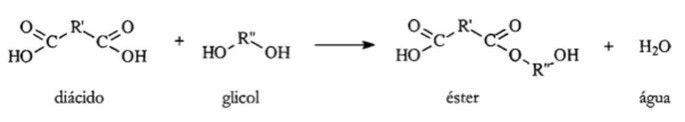
Na polimerização por condensação, monômeros bifuncionais (com dois grupos funcionais reativos) reagem entre si, formando a ligação entre unidades e, simultaneamente, liberando uma molécula pequena como subproduto (água, amônia, HCl, etc.). Por exemplo, um diácido carboxilico reage com um glicol formando poliéster e água.
Questão 6
O processo de vulcanização da borracha natural, descoberto por Charles Goodyear, tem como principal finalidade:
a) Tornar a borracha mais solúvel em solventes orgânicos.
b) Introduzir ligações cruzadas (pontes de enxofre) entre as cadeias poliméricas.
c) Quebrar as cadeias longas do polímero para torná-lo mais maleável.
d) Adicionar plastificantes para aumentar sua flexibilidade.
Resposta: alternativa B.
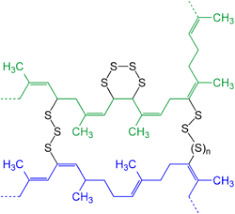
A vulcanização é um processo químico no qual se adiciona enxofre à borracha natural (poli-isopreno) sob calor. O enxofre forma ligações cruzadas (pontes de enxofre, -S-S-) entre as cadeias poliméricas lineares. Isso confere ao material maior resistência mecânica, elasticidade recuperável (pois as ligações cruzadas "puxam" a cadeia de volta após a deformação) e menor sensibilidade às variações de temperatura.
Questão 7
Um polímero cuja cadeia principal contém o grupo funcional éster (-COO-) é o:
a) Polipropileno (PP).
b) Policloreto de vinila (PVC).
c) Poliestireno (PS).
d) Politereftalato de etileno (PET).
Resposta: alternativa D.
O PET é um poliéster. Sua unidade de repetição é formada a partir do monômero etilenoglicol (um diálcool) e do ácido tereftálico (um diácido), resultando em uma cadeia principal que contém a função éster (-COO-).
Os outros polímeros listados possuem cadeias formadas apenas por carbonos: PP (hidrocarboneto), PVC (halogenado) e PS (hidrocarboneto aromático).
Questão 8
A persistência de polímeros sintéticos como o polietileno no ambiente deve-se principalmente ao fato de:
a) Possuírem cadeias muito curtas e hidrofílicas.
b) Serem quimicamente inertes e resistentes à ação de microrganismos decompositores.
c) Dissolverem-se facilmente na água da chuva.
d) Possuírem grupos funcionais que reagem rapidamente com o oxigênio do ar.
Resposta: alternativa B.
A grande maioria dos polímeros sintéticos de grande consumo (como PE, PP, PS, PET) possui cadeias longas e estáveis, formadas principalmente por ligações C-C e C-H, que são quimicamente inertes em condições ambientais. Além disso, suas estruturas compactas e hidrofóbicas não são reconhecidas ou facilmente quebradas pelas enzimas dos microrganismos decompositores encontrados na natureza, resultando em um tempo de degradação extremamente longo (centenas de anos).
Saiba mais em Polímeros: o que são, tipos, exemplos e biodegradáveis.
ALVES, Gustavo. Exercícios sobre polímeros (com respostas explicadas). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/exercicios-sobre-polimeros-com-respostas-explicadas/. Acesso em:


