O que é isomeria e exemplos de isômeros
A isomeria é um fenômeno observado quando diferentes compostos são formados por quantidades iguais dos mesmos tipos de átomos.
Sendo assim, podemos encontrar substâncias químicas com a mesma fórmula molecular e distintas fórmulas estruturais ou arranjos espaciais.
Na Química Orgânica muitos compostos orgânicos apresentam isômeros. Como cada átomo de carbono pode fazer 4 ligações químicas, é possível observar diversas combinações.
A mudança no arranjo dos átomos faz surgir novas substâncias e, consequentemente, as propriedades físicas e químicas são diferentes.
Quando dizemos que compostos são isômeros significa que eles apresentam partes iguais, pois a palavra é a combinação de dois termos de origem grega: isos, quer dizer “mesmo”, e meros, que é “partes”.
Os tipos de isômeros são divididos em dois grandes grupos: isomeria plana e isomeria espacial (estereoisomeria).
A isomeria plana pode ser visualizada pela fórmula estrutural plana dos compostos e apresenta cinco classes: de posição, de função, de cadeia, de compensação e tautomeria.
A isomeria espacial é observada pela orientação dos compostos e se subdivide em geométrica (cis-trans) e óptica.
O conceito de isomerismo foi introduzido em 1830 pelo cientista sueco Jacob Berzelius.
Exemplos de isômeros
A isomeria de cadeia ocorre quando o mesmo conjunto de átomos se conectam formando estruturas do mesmo grupo funcional, mas com cadeias diferentes.
Exemplo: a fórmula molecular C4H10 de um hidrocarboneto pode se apresentar com uma cadeia linear ou ramificada.
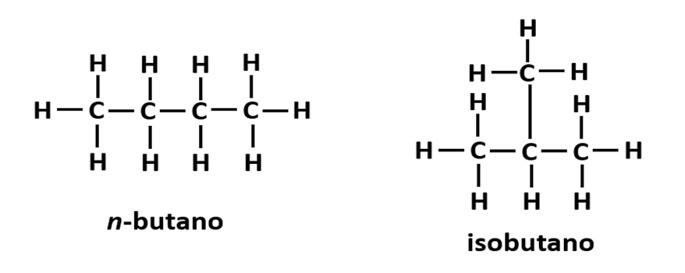
A isomeria de posição ocorre quando os compostos são formados pelos mesmos grupos funcionais, mas eles estão em diferentes posições na cadeia.
Exemplo: A fórmula molecular C4H9OH corresponde a dois tipos de álcool.
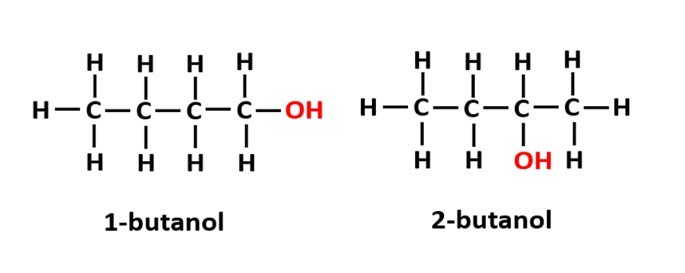
A isomeria de função ocorre quando a mesma fórmula molecular corresponde a dois compostos com diferentes grupos funcionais.
Exemplo: A fórmula molecular C2H6O corresponde a dois isômeros que apresentam as funções álcool (-OH) e éter (-O-).
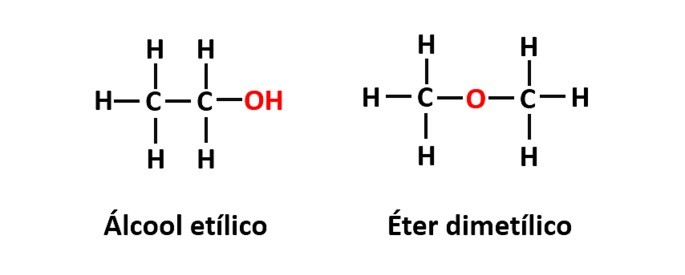
A isomeria de compensação ocorre quando existe um heteroátomo na cadeia e ele ocupa diferentes posições. Trata-se de um caso particular da isomeria de posição.
Exemplo: A fórmula molecular C4H10O indica a presença de um átomo de oxigênio na cadeia, mas a sua posição pode mudar e formar diferentes compostos.
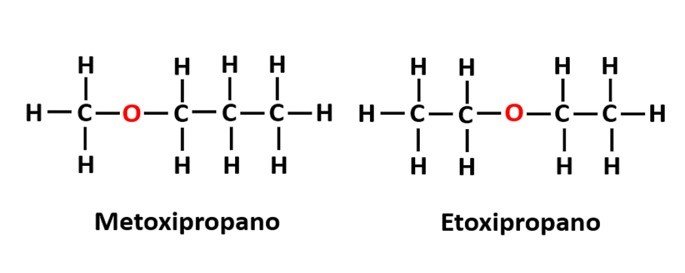
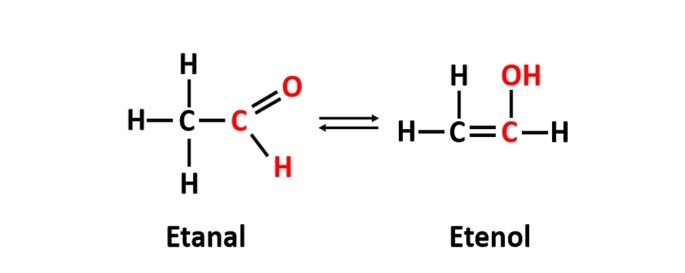
A isomeria dinâmica, também chamada de tautomeria, ocorre quando dois compostos com funções diferentes estão na mesma solução em equilíbrio dinâmico.Trata-se de um caso particular da isomeria de função.
Exemplo: A fórmula molecular C2H4O corresponde aos compostos com as funções aldeído e enol.
Saiba mais sobre a isomeria plana.
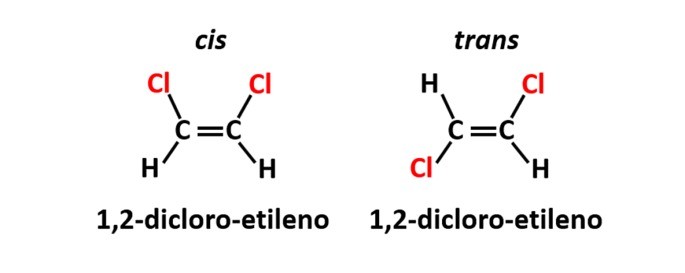
A isomeria geométrica, também chamada de isomeria cis-trans, ocorre quando a presença de uma ligação dupla ou estrutura cíclica faz com que ligantes iguais estejam do mesmo lado do plano (cis) ou em lados opostos (trans).
Exemplo: os átomos de cloro nos compostos de fórmula molecular C2H2Cl2 podem apresentar duas estruturas espaciais.
A isomeria óptica ocorre quando ao desviar a luz polarizada emitida sobre a estrutura, os compostos conseguem desviar o feixe luminoso para esquerda, se for um isômero levogiro (l), ou para a direita, quando é um isômero dextrogiro (d).
Exemplo: Este tipo de isomeria ocorre com o ácido lático. Observe a seguir que as imagens espectrais dos isômeros não se sobrepõem, por isso são chamados de enantiômeros.
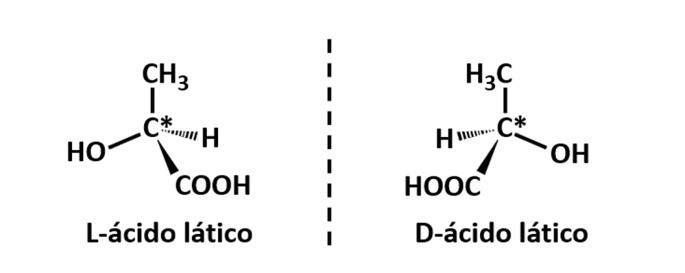
O símbolo C* indica a presença de um carbono quiral na estrutura, ou seja, um átomo de carbono com 4 ligantes diferentes.
Saiba mais sobre a isomeria com os conteúdos:
- Tipos de isomeria
- Isomeria espacial
- Isomeria geométrica
- Isomeria óptica
- Exercícios sobre isomeria plana
- Exercícios sobre isomeria geométrica (com respostas resolvidas)
- Carbono quiral ou assimétrico: entenda o que é e como identificar (com exercícios)
- Exercícios sobre carbono quiral ou assimétrico (com questões resolvidas)
BATISTA, Carolina. O que é isomeria e exemplos de isômeros. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/o-que-e-isomeria/. Acesso em:

