Hidrocarbonetos: quais são, classificação e nomenclaturas (com exemplos)
Os hidrocarbonetos são compostos formados apenas por carbono e hidrogênio, com fórmula geral: CxHy.
Trata-se de uma extensa quantidade de substâncias, cujo as mais conhecidas são constituintes do petróleo e gás natural.
A cadeia principal de um hidrocarboneto é formada de carbono e, por sua vez, os átomos de hidrogênio se ligam por meio de ligação covalente.
São largamente utilizados na indústria química, sendo essenciais na produção dos derivados do petróleo: combustíveis, polímeros, parafinas, dentre outros.
O que você vai encontrar neste conteúdo:
- Propriedades dos hidrocarbonetos
- Classificação dos hidrocarbonetos
- Nomenclatura dos hidrocarbonetos
- Tipos de hidrocarbonetos
- Resumo sobre os hidrocarbonetos
- Exercícios
Propriedades dos hidrocarbonetos
| Interação molecular | São compostos praticamente apolares e suas moléculas se unem por dipolo induzido. |
|---|---|
| Ponto de fusão e ebulição | São baixos em comparação aos compostos polares. |
| Estados de agregação |
|
| Densidade | Possuem densidade menor que a da água. |
| Solubilidade | São insolúveis em água e solúveis em substâncias apolares. |
| Reatividade |
|
Classificação dos hidrocarbonetos
Quanto à forma da cadeia carbônica principal, os hidrocarbonetos são classificados em:
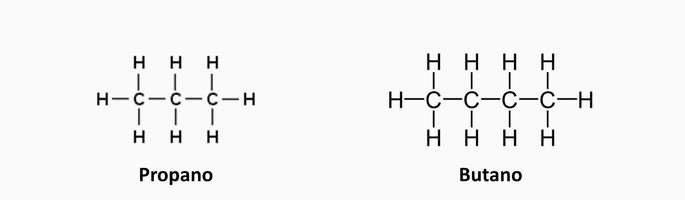
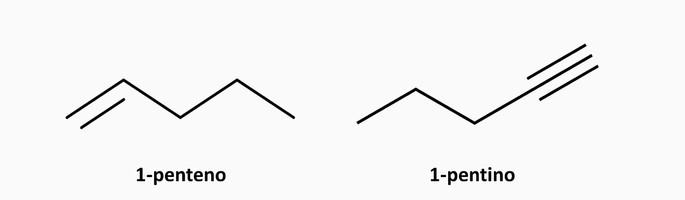
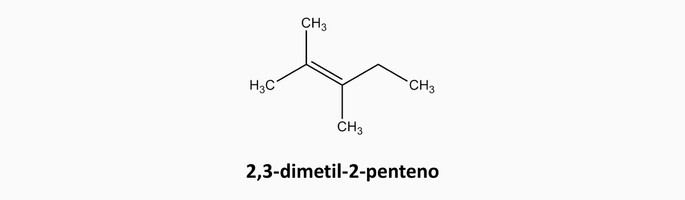
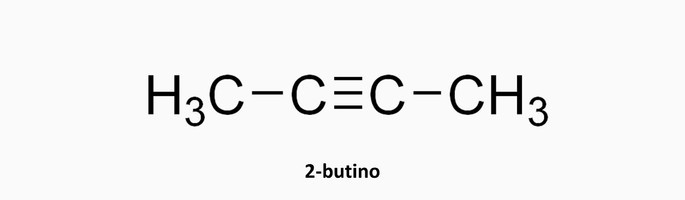
Hidrocarbonetos alifáticos
Formados por cadeias carbônicas abertas ou acíclicas, as quais possuem carbonos terminais.
- Alcanos
- Alcenos
- Alcinos
- Alcadienos
Exemplo:
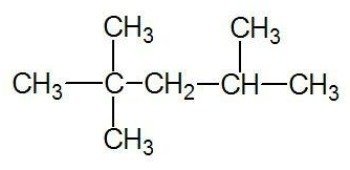
Veja também: cadeias carbônicas
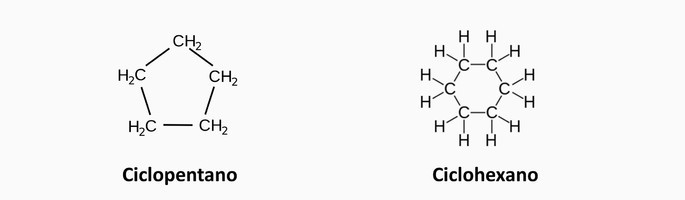
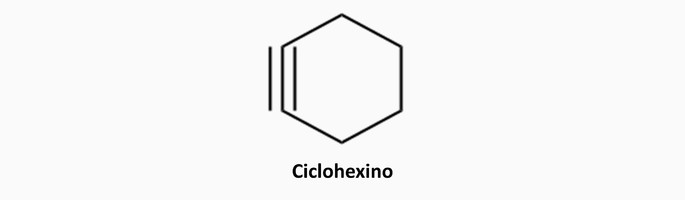
Hidrocarbonetos cíclicos
Formados por cadeia carbônica fechada ou cíclica as quais não possuem carbonos terminais.
- Ciclanos
- Ciclenos
- Ciclinos
- Aromáticos
Exemplos:
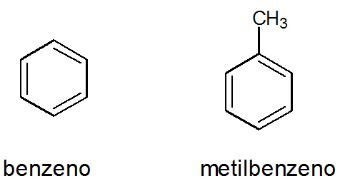
Veja também: benzeno
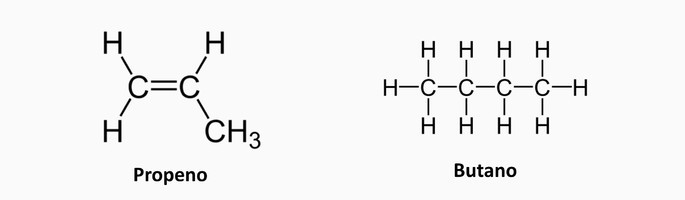
Quanto às ligações das cadeias carbônicas, sejam elas simples, duplas ou triplas:
Hidrocarbonetos saturados
Os compostos são formados por ligações simples entre os átomos de carbono e hidrogênio.
- Alcanos
- Ciclanos
Exemplo:
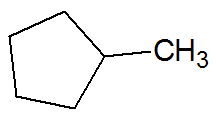
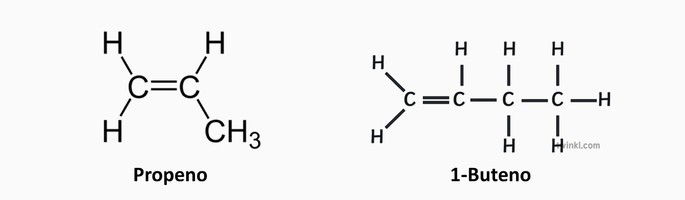
Hidrocarbonetos insaturados
Os compostos formados possuem ligações duplas ou triplas entre os átomos de carbono.
- Alcenos
- Alcinos
- Alcadienos
- Ciclenos
- Ciclinos
- Aromáticos
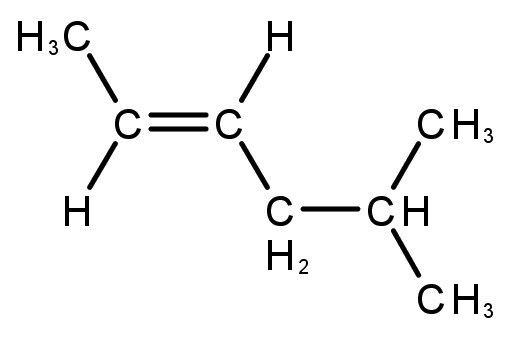
Leia também sobre:
Nomenclatura dos hidrocarbonetos
A nomenclatura dos hidrocarbonetos é definida através dos seguintes termos:
| PREFIXO | INTERMEDIÁRIO |
SUFIXO |
|---|---|---|
| Indica o número de carbonos presentes na cadeia. | Tipo de ligação encontrada na cadeia. | Identificação do grupo funcional. |
| PREFIXO | INTERMEDIÁRIO | SUFIXO | ||
|---|---|---|---|---|
| 1 C | MET | Apenas ligação simples | AN | O |
| 2 C | ET | |||
| 3 C | PROP | Uma ligação dupla | EN | |
| 4 C | BUT | |||
| 5 C | PENT | Duas ligações duplas | DIEN | |
| 6 C | HEX | |||
| 7 C | HEPT | Uma ligação tripla |
IN |
|
| 8 C | OCT | |||
| 9 C | NON | Duas ligações triplas | DIIN | |
| 10 C | DEC | |||
Exemplos
Acompanhe como ocorre a formação dos nomes de hidrocarbonetos:
| Etano |
- Prefixo: ET, que corresponde à 2 carbonos.
- Intermediário: AN, que corresponde à ligações simples.
- Sufixo: O, que corresponde à função hidrocarboneto.
Observe os demais exemplos:
| Propano | |
| Eteno | |
| Etino | |
| Propadieno |
Em alguns casos é preciso indicar a posição da ligação dupla ou tripla. A numeração deve iniciar a partir da extremidade mais próxima dessa ligação.
| 1,3-butadieno | |
| 1-butino |
Saiba mais em:
Tipos de Hidrocarbonetos
Confira os principais tipos de hidrocarbonetos, suas características e os compostos utilizados:
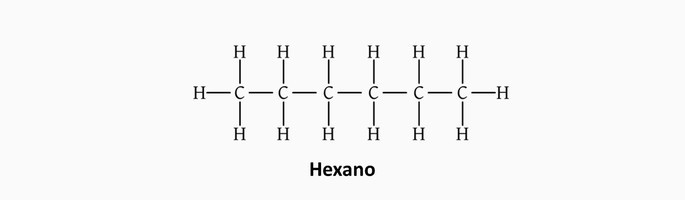
Alcanos
São hidrocarbonetos de cadeia aberta com ligações simples entre os átomos de carbono e hidrogênio, cuja fórmula geral é CnH2n+2.
Características dos alcanos
- Também são chamados de parafinas ou parafínicos.
- São encontrados na natureza no gás natural e no petróleo.
- São utilizados como combustíveis: gás de cozinha, gasolina, óleo diesel, etc.
Exemplos de alcanos
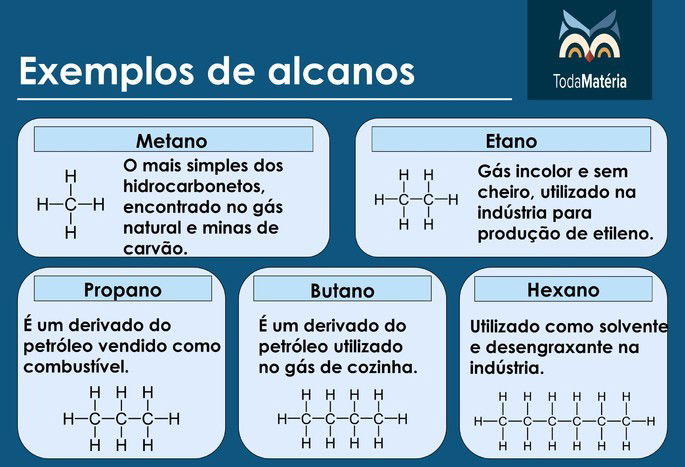
Alcenos
São hidrocarbonetos de cadeia aberta e possuem ligação dupla, cuja fórmula geral é CnH2n.
Características dos alcenos
- Também são chamados de olefinas, alquenos ou hidrocarbonetos etilênicos.
- São obtidos industrialmente a partir do craqueamento de alcanos presentes no petróleo.
- São utilizados como matéria-prima na indústria: plásticos, corantes, explosivos, etc.
Exemplos de alcenos
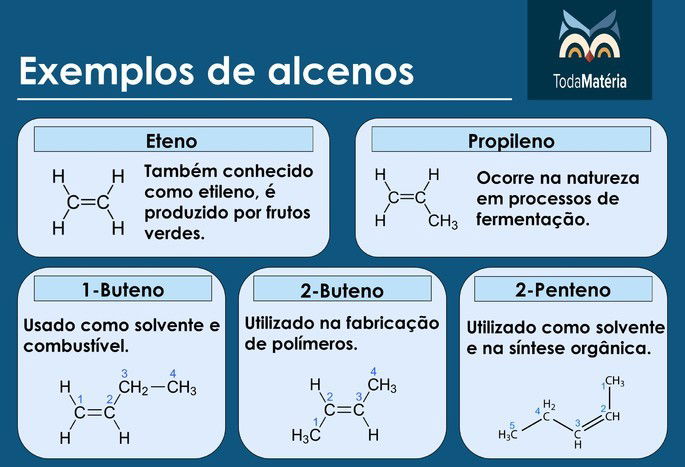
Alcinos
São hidrocarbonetos de cadeia aberta e presença de ligação tripla, cuja fórmula geral é CnH2n-2.
Características dos alcinos
- São mais reativos que os alcanos e alcenos devido a ligação tripla.
- Os alcinos com mais de 14 átomos de carbono são sólidos.
- O alcino mais utilizado é o acetileno, comumente empregado na produção de borrachas sintéticas, fibras têxteis e plásticos.
Exemplos de alcinos
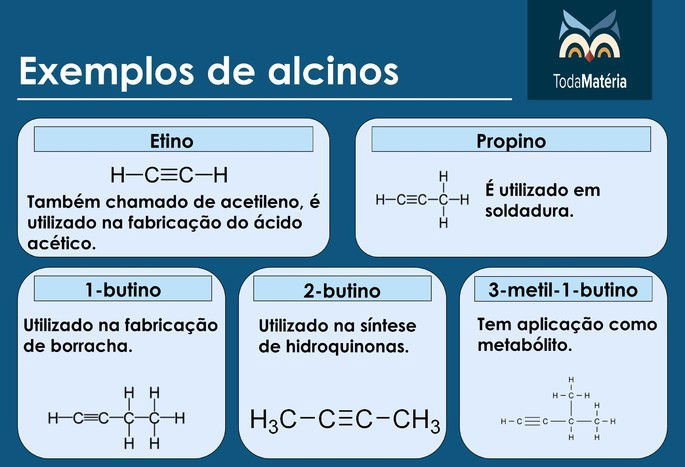
Alcadienos
São hidrocarbonetos de cadeia aberta e presença de duas ligações duplas, cuja fórmula geral é CnH2n-2
Características dos alcadienos
- Também chamados de dienos ou diolefinas
- Na natureza são encontrados nos terpenos, extraídos de óleos essenciais de frutas.
- O composto mais conhecido é o isopreno, encontrado na borracha natural e óleos essenciais.
Exemplos de alcadienos
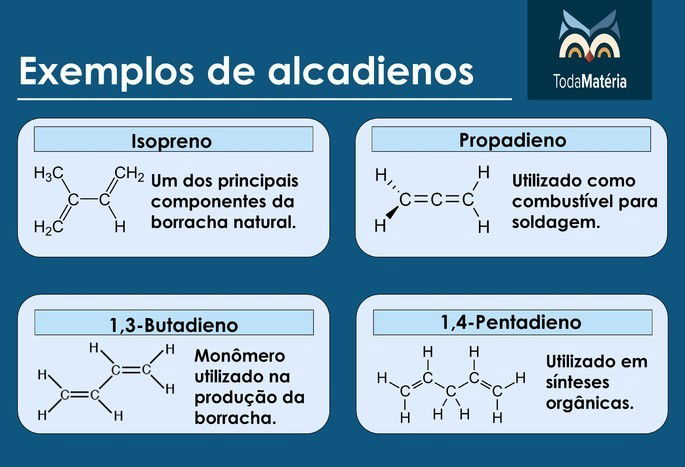
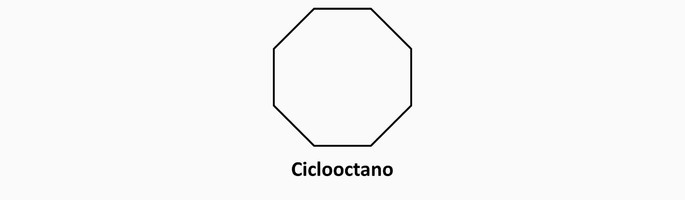
Ciclanos
São hidrocarbonetos de cadeia fechada com ligações simples entre os átomos de carbono e hidrogênio, cuja fórmula geral é CnH2n.
Características dos ciclanos
- Também são chamados de cicloalcanos ou cicloparafinas.
- São instáveis quando submetidos à elevadas pressões.
- Cadeias com mais de 6 carbonos são estáveis, enquanto que com menos de 5 carbonos são reativas.
Exemplos de ciclanos
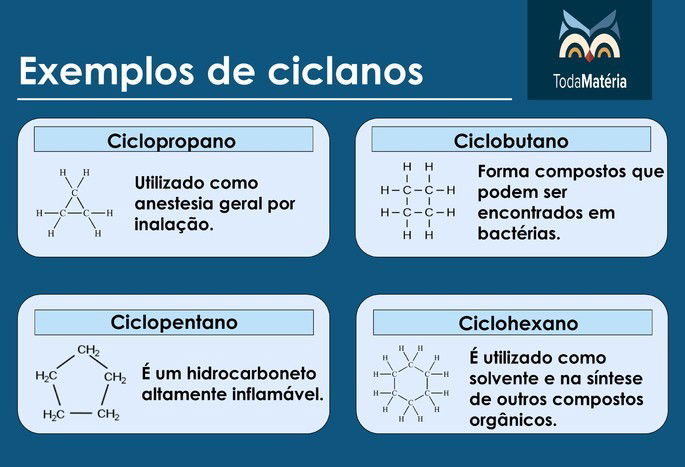
Ciclenos
São hidrocarbonetos de cadeia fechada e com a presença de ligação dupla, cuja fórmula estrutural é CnH2n-2.
Características dos ciclenos
- Também são chamados de cicloalcenos.
- Compostos de 3 à 5 carbonos são instáveis.
- São geralmente encontrados no gás natural, óleo e petróleo.
Exemplos de ciclenos
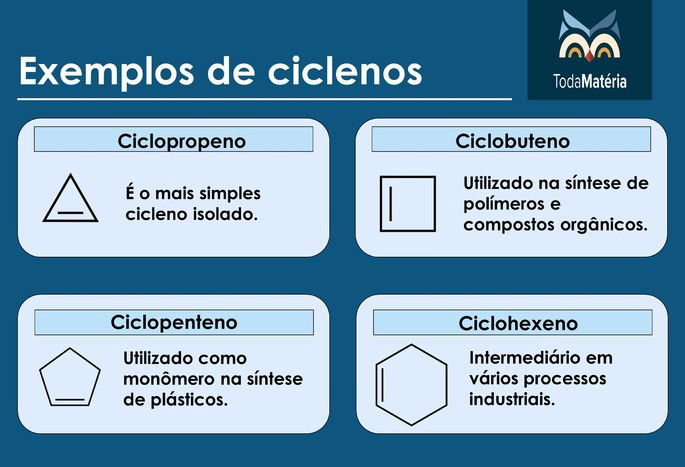
Ciclinos
São hidrocarbonetos de cadeia fechada e com a presença de ligação tripla, cuja fórmula estrutural é CnH2n-4.
Características dos ciclinos
- Também são chamados de cicloalcinos ou cicloalquinos.
- São hidrocarbonetos cíclicos e insaturados.
- São instáveis devido a ligação tripla e não são encontrados na natureza.
Exemplos de ciclinos
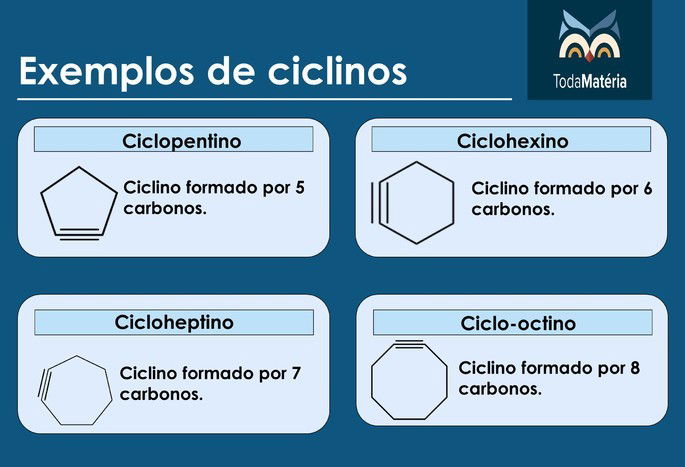
Aromáticos
São hidrocarbonetos de cadeia fechada com ligações simples e duplas alternadas.
Características dos aromáticos
- Também são chamados de arenos.
- São compostos insaturados, pois apresentam 3 ligações duplas.
- São constituídos de no mínimo um anel aromático.
Exemplos de aromáticos
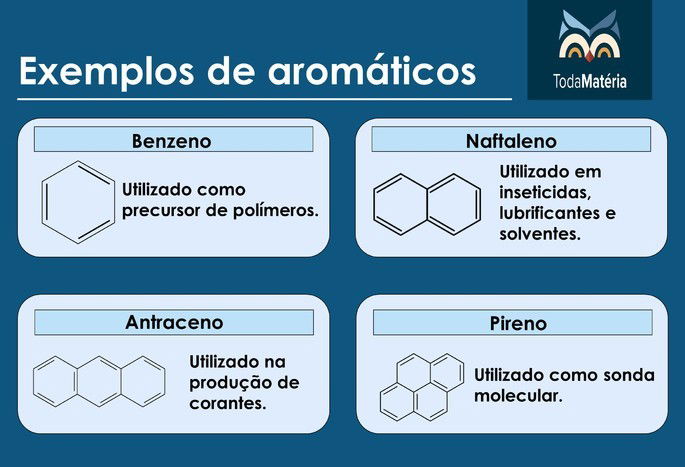
Você também pode se interessar por:
Resumo sobre Hidrocarbonetos
| Função |
Fórmula Geral |
Características |
|---|---|---|
| Alcano |
Cadeia aberta com ligações simples. |
|
| Alceno | Cadeia aberta com ligação dupla. | |
| Alcino | Cadeia aberta com ligação tripla. | |
| Alcadieno | Cadeia aberta com duas ligações duplas. | |
| Ciclanos | Cadeia fechada com ligações simples. | |
| Ciclenos | Cadeia fechada com ligação dupla. | |
| Ciclinos | Cadeia fechada com ligação tripla. | |
| Aromático | Variável | Cadeia fechada com ligações simples e duplas alternadas. |
Mapa Mental sobre Hidrocarbonetos
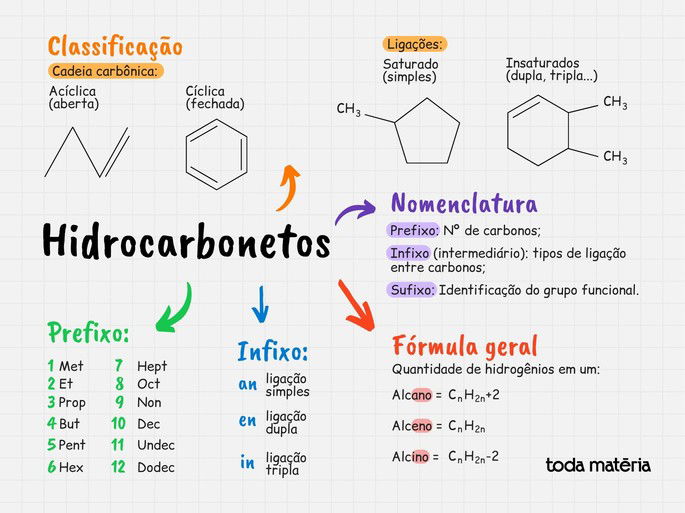
Exercícios sobre Hidrocarbonetos
1. (UEMA) GLP (Gás Liquefeito de Petróleo), também conhecido popularmente como gás de cozinha, é um combustível fóssil não renovável que pode se esgotar de um dia para o outro, caso não seja utilizado com planejamento e sem excesso. Ele é composto, dentre outros gases, por propano C3H8, butano C4H10 e pequenas quantidades de propeno C3H6 e buteno C4H8. Esses compostos orgânicos são classificados como hidrocarbonetos que apresentam semelhanças e diferenças entre si. Com base no tipo de ligação entre carbonos e na classificação da cadeia carbônica dos compostos acima, pode-se afirmar que :
a) os compostos insaturados são propano e butano.
b) os compostos insaturados são propeno e buteno.
c) os compostos insaturados são propeno e butano.
d) os compostos apresentam cadeias homocíclicas.
e) os compostos possuem cadeias heterocíclicas.
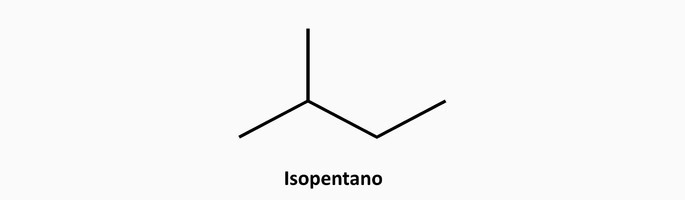
2. (Uel) Um dos hidrocarbonetos de fórmula C5H12 pode ter cadeia carbônica:
a) cíclica saturada.
b) acíclica heterogênea.
c) cíclica ramificada.
d) aberta insaturada.
e) aberta ramificada.
3. (PUC) Alcinos são hidrocarbonetos:
a) alifáticos saturados.
b) alicíclicos saturados.
c) alifáticos insaturados com dupla ligação.
d) alicíclicos insaturados com tripla ligação.
e) alifáticos insaturados com tripla ligação.
Quer continuar testando os seus conhecimentos? Não deixe de ver essas listas:
- Exercícios sobre Hidrocarbonetos
- Exercícios sobre nomenclatura de hidrocarbonetos
- Exercícios sobre Química Orgânica
- Exercícios sobre Funções Orgânicas
Referências Bibliográficas
McMURRY, J., Química Orgânica vol. 1 e vol. 2. Editora CENGAGE Learning. Tradução da 6ª Edição Norte Americana, 2008KOTZ, John C.; TREICHE
CASTILHO, Rubens. Hidrocarbonetos: quais são, classificação e nomenclaturas (com exemplos). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/hidrocarbonetos/. Acesso em: